Большая устойчивость
Cтраница 3
Большая устойчивость димерной формы по сравнению с устойчивостью мономерной с неполным числом электронов, несомненно, обязана существованию нескольких резонансных форм А12С16, которые содействуют его устойчивости. На основании приведенной выше электронной структуры нужно было бы ожидать, что только мономерный хлористый алюминий образует комплексы с органическими соединениями. Однако в реакциях Фриделя-Крефтса допускают, что комплексы образуются между А1С1а или А12С16 и одним или со всеми наличными компонентами: ароматическим углеводородом, органическим галоидным соединением и продуктами реакции. [31]
Большая устойчивость бензоилуксусной кислоты обусловлена ее енольным строением. Последнее определяет и устойчивость оксалилуксус-ной кислоты. [32]
Большая устойчивость тиглиновой кислоты понятна, так как она содержит две СН3 - группы при СС-связи. [33]
Большая устойчивость открытой формы, по-видимому, обусловливается также и энтропийным фактором, так как весьма вероятно, что энтропия предельных циклических соединений меньше, чем энтропия соединений с открытой цепью, имеющих тот же состав. [34]
Отмеченная большая устойчивость этилендиаминовых комплексов по сравнению с аммиачными - явление общее в химии комплексных соединений. Эта закономерность, подчеркивающая стабиливирующее действие циклических заместителей типа этилендиамина, характерна не только для соединений кобальта, но отчетливо обнаруживается и на соединениях других, металлов. [35]
Отмеченная большая устойчивость этилендиаминовых комплексов по сравнению с аммиачными - явление общее в химии комплексных соединений. Эта закономерность, подчеркивающая стабилизирующее действие циклических заместителей типа этилендиамина, характерна не только для соединений кобальта, но отчетливо обнаруживается и на соединениях других металлов. [36]
Большая устойчивость низших степеней окисления у самых тяжелых элементов наблюдается не только в группе III Б у таллия, ко и в группах IV Б и V Б у свинца и висмута. [37]
Большая устойчивость низших степеней окисления у самых тяжелых элементов наблюдается не только в группе III Б у таллия, но и в группах IV Б и V Б у свинца и висмута. Сиджвик заметил это в 1933 г. и в качестве объяснения предположил наличие у это-мов этих элементов инертной пары электронов. Гримм и Зоммер-фельд считали, что большая устойчивость низшей степени окисления этих элементов обусловлена стабилизацией вследствие заполнения ns - уровня. Однако ионизационные потенциалы не подтверждают этой точки зрения. [38]
Большая устойчивость эмиссии окиси тория ведет к тому, что катод не так быстро отравляется и может работать при плохом вакууме. Последнее объясняется тем, что свободный торий образуется и при рабочей температуре, что компенсирует его отравление. Оксидно-ториевый катод допускает отбор весьма больших плотностей тока в непрерывном режиме и хорошо работает в режиме насыщения. [39]
Большая устойчивость димеров карбоновых кислот позволяет ставить вопрос о колебаниях этого комплекса. Частоты колебаний одной половины комплекса относительно другой должны проявляться в низкочастотной области спектра, так как энергия связи димеров по сравнению с обычными химическими связями невелика. [40]
Большая устойчивость низших степеней окисления у самых тяжелых элементов наблюдается не только в группе III Б у таллия, ко и в группах IV Б и V Б у свинца и висмута. [41]
Большая устойчивость растворов низкозамещенных ксан-тогенатов, содержащих очень мало лиофильных дитиокарбонатных групп, объясняется, по-видимому, относительно малыми количествами коагулирующих солей в этих растворах и другими факторами. [42]
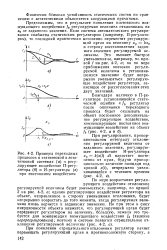 |
Примеры переходных процессов в статической и астатической системах ( а и регулирующее воздействие П - регу. [43] |
Физически большая устойчивость статических систем по сравнению с астатическими объясняется следующими причинами. [44]
Большая устойчивость енольной формы фенолов вызвана более высокой степенью сопряжения по сравнению с кетонной формой. [45]
Страницы: 1 2 3 4