Относительная устойчивость - комплекс
Cтраница 1
Относительная устойчивость комплекса ( 8) отчасти обусловлена наличием аниона Вр4 в ионной паре ( ср. Выделение этого комплекса не доказывает, что подобные интермедиа обязательно образуются в реакциях нитрования с использованием нитрующей смеси, но в совокупности с кинетическими и другими данными участие таких частиц кажется чрезвычайно вероятным. [1]
При невысокой относительной устойчивости комплекса, когда неравенства (1.15) и (1.16) не соблюдаются, необходимая степень связанности определяемого иона в окрашенное соединение обеспечивается избытком фотометрического реагента. [2]
При невысокой относительной устойчивости комплекса, когда неравенства (1.8) к (1.9) не соблюдаются, необходимая степень связанности определяемого иона в окрашенное соединение обеспечивается избытком фотометрического реагента. [3]
Выводы об относительной устойчивости комплексов ионов металлов часто делаются только на основании изменений свободной энергии при комплексообразовании. Поскольку комплексообразованию благоприятствуют положительные изменения энтропии и отрицательные значения теплосодержания [ уравнение ( 27) ], для более полного понимания необходимо рассматривать эти функции по отдельности. [4]
Для качественной оценки относительной устойчивости комплексов как в основном, так и в возбужденном состоянии используются рассматриваемые значения Лмакс вместо истинных констант равновесия, которые для аддуктов парациклофанов определить не удалось из-за ограниченных количеств доноров. [5]
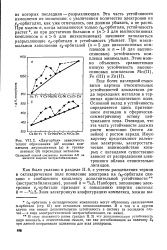
Еще более наглядной становится картина относительных устойчивостей комплексов ряда переходных металлов в терминах кристаллического поля. Основной вклад в устойчивость определяется здесь притяжением лигандов к сферически-симметричному остову центрального иона. Очевидно, что эта часть устойчивости должна расти монотонно ( почти линейно) с ростом заряда. Иную картину представляют валентные электроны, электростатическое взаимодействие которых с лигандами существенно зависит от распределения электронного облака относительно лигандов. [7]
Давно уже стало обычным оценивать относительную устойчивость малостабильных комплексов по их относительной летучести. Донор-ная способность фосфора в большей степени снижается виниль-ной группой, чем этильной. [8]
 |
Изменение равновесного состава смеси этилбен - I. [9] |
Используя найденные значения констант равновесия реакций ( 1) и ( 2), а также данные об относительной устойчивости комплексов различных этилбензолов, Мак-Коли и Лин [132] рассчитали равновесные составы смесей этилбензолов в присутствии избытка трехфтористого бора в зависимости от соотношения числа этильных групп и бензольных ядер. [10]
В присутствии фтор-ионов Fe ( III) можно определять с помощью другого реагента, например, салициловой кислоты, с которой ионы Fe ( III) образуют более прочный салицилатный комплекс. Правда, при рН 3 относительная устойчивость моносалицилатного комплекса Fe ( III) сравнительно невелика фнезаи - 1 1 Ю8) и мешающее влияние фтор-ионов можно устранить только в том случае, если общая равновесная концентрация салициловой кислоты будет превышать концентрацию фтор-ионов не менее, чем в 1 5 - Ю4 раз. Если же фотометрическое определение Fe ( III) проводить в виде трисалицилатного комплекса при рН 10 ( Ppesais - 2 - Ю12), то мешающее влияние фтор-ионов удается полностью устранить. [11]
В присутствии фтор-ионов Fe ( III) можно определять с помощью другого реагента, например, салициловой кислоты, с которой ионы Fe ( III) образуют более прочный салицилатный комплекс. Правда, при рН 3 относительная устойчивость моносалицилатного комплекса Fe ( III) сравнительно невелика ( Ррезаи - 1 1 - 105) и мешающее влияние фтор-ионов можно устранить только в том случае, если общая равновесная концентрация салициловой кислоты будет превышать концентрацию фтор-ионов не менее, чем в 1.5 - 104 раз. Если же фотометрическое определение Fe ( III) проводить в виде трисалицилатного комплекса при рН 10 ( Рре3а1з - 2 - Ю12), то мешающее влияние фтор-ионов удается полностью устранить. [12]
Однако имеются явные различия в случае индивидуальных металлов. Например, для никеля, кобальта, кадмия относительная устойчивость комплексов указанных трех красителей располагается в ряд: N S О. Для цинка наблюдается следующий порядокг N О S и в случае меди: N S О. [13]
Если реакции протекают слева направо, то можно сказать, что для этих систем А более сильная кислота, чем А, а В более сильное основание, чем В. Относительная сила кислоты или основания затем может быть выражена с помощью относительной устойчивости кислотно-основных комплексов. [14]
Такая точка зрения не допускает переноса заряда между лигандами и центральным атомом, что противоречит ряду экспериментальных результатов, полученных методами дифракции нейтронов, электронного парамагнитного резонанса и ядерного магнитного резонанса. Кроме того, недостатком теории кристаллического поля является то, что она не позволяет правильно понять причину изменения относительной устойчивости комплексов при изменении лигандного окружения, а также описывать двойные связи между лигандами и центральным ионом, которые часто способствуют повышению устойчивости комплексов. [15]
Страницы: 1 2