Относительная устойчивость - комплекс
Cтраница 2
Относительным критерием электроотрицательности металла является тенденция этих соединений к образованию комплексных ионов. Соединения такого типа недостаточно ионизированы в эфире и скорее представляют собой ассоциированный комплекс, чем истинную соль. Относительную устойчивость комплексов можно продемонстрировать на примере скорости металлирования флуорена, который быстро металли-руется фениллитием, но совсем не металлируется диалкилпро-изводными элементов II группы. Литийтрифенилбериллий не реагирует с флуореном в течение 2 недель. Остальные соединения реагируют со все возрастающей скоростью в порядке LiZn ( C6H5b, LiMg ( C6H5) 3, иСсЦСбНзЬ - Таким образом, бериллий образует наиболее устойчивый комплекс, кадмий - наименее устойчивый, а ртуть совсем не образует комплекса; следовательно, не существует определенной зависимости от величины электроотрицательности. [16]
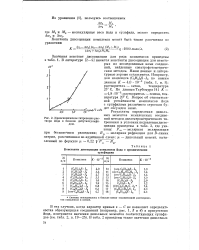 |
Криоскопическое титрование рас-твора йода в бензоле дибутилсульфи. [17] |
Наши данные и литературные хорошо согласуются. По данным Тсубомура [4] К 4 8 10 - 3; растворитель - гептан, температура 20 С. Вопрос об относительной устойчивости комплексов йода с сульфидами различного строения будет обсужден ниже. [18]
В специальных условиях удалось получить некоторые комплексные соединения щелочных металлов с такими кислородсодержащими лигандами, как салициловый альдегид и дибензоилметан. Согласно данным Брэди и, литий, натрий и калий образуют с салициловым альдегидом комплексы, в которых на один ион щелочного металла приходятся две молекулы салицилового альдегида, а рубидий и цезий - комплексы с тремя молекулами салицилового альдегида. В 1954 г. Фернелиус и Ван - Уйтерт12 опубликовали заметку об относительной устойчивости комплексов щелочных металлов с ди-бензоилметаном. [19]
В специальных условиях удалось получить некоторые комплексные соединения щелочных металлов с такими кислородсодержащими лигандами, как салициловый альдегид и дибензоилметан. Согласно данным Брэди п, литий, натрий и калий образуют с салициловым альдегидом комплексы, в которых на один ион щелочного металла приходятся две молекулы салицилового альдегида, а рубидий и цезий - комплексы с тремя молекулами салицилового альдегида. В 1954 г. Фернелиус и Ван - Уйтерт12 опубликовали заметку об относительной устойчивости комплексов щелочных металлов с ди-бензоилметаном. [20]
Различные факторы, определяющие тип присоединения в каждом конкретном случае, до конца не выяснены. Имеют большое значение все факторы - стерическое сжатие, сольватация и делокализа-ция в изомерных комплексах, а также в переходных состояниях, ведущих к этим комплексам. Эти факторы во многих случаях связаны друг с другом, что осложняет объяснение относительной устойчивости комплекса. Некоторые нуклеофилы присоединяются к электронодефицитным ароматическим соединениям только в незамещенное положение, в то время как другие присоединяются только в замещенное положение. Направление атаки часто зависит от природы растворителя. Рассмотрим относительное значение некоторых факторов, влияющих на устойчивость изомерных комплексов. [21]
Там, где элементы характеризуются постоянной валентностью, сравнение производить легко. Если же элементы проявляют переменную валентность, то, строго говоря, их можно сравнивать между собой лишь в одинаковом валентном состоянии. Если условно выбрать для сравнения признак устойчивости в водном растворе, численно выражаемый величиной константы нестойкости, то можно видеть, что в зависимости от природы лиганда, относительная устойчивость комплексов Си 1 и Ag может быть различной. [22]
Там, где элементы характеризуются постоянной валентностью, сравнение производить легко. Если же элементы проявляют переменную валентность, то, строго говоря, их можно сравнивать между собой лишь в одинаковом валентном состоянии. Если условно выбрать для сравнения признак устойчивости в водном растворе, численно выражаемый величиной константы нестойкости, то можно видеть, что в зависимости от природы лиганда, относительная устойчивость комплексов Си и Ag может быть различной. [23]
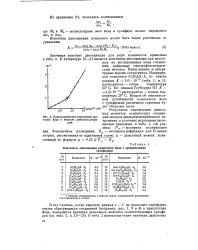 |
Криоскопическое титрование раствора йода в бензоле дибутилсульфи-дом. [24] |
В литературе [2-4] имеются константы диссоциации для некоторых из исследованных нами соединений, найденные спектрофотометриче-ским методом. Наши данные и литературные хорошо согласуются. По данным Тсубомура [4] К 4 8 10 - 3; растворитель - гептан, температура 20 С. Вопрос об относительной устойчивости комплексов йода с сульфидами различного строения будет обсужден ниже. [25]
Было найдено, что скорость обменной реакции меди с Ni-EDTA значительно больше, хотя уравнения для скорости реакции аналогичны [184] В этом случае А il 65 - 10 - 2 л / молъ-сек. Если предполагается аналогичный механизм, то вполне вероятно, что k в уравнении (3.110) не должно значительно различаться для меди и цинка. Следовательно, разницу в скорости реакции в 6500 раз должны определять значения К. Видно, что относительная устойчивость иминодиацетатных комплексов довольно хорошо согласуется с относительной реакционной способностью. [26]
В дальнейшем основное внимание было обращено на исследование процессов образования ацетатных и смешанных окси-ацетатных комплексов трехвалентного железа непосредственно в растворах. Михаэлис и Фридгейм [16], изучив большое количество систем, включающих комплексы трех - и двухвалентного железа с различными анионами, установили, что каждый комплекс существует в определенной области рН и что в зависимости от природы комплексообразующего адден-да окислительный потенциал меняется в довольно широком интервале. Ими также показано, что ионы трехвалентного железа обладают большей тенденцией к комплексообразова-нию, чем ионы двухвалентного железа. Как правило, в том случае, когда аддендом является анион, комплексы Fe3 более устойчивы, чем комплексы Fe2, и относительная устойчивость комплекса увеличивается с зарядом адденда. [27]
Что же касается корреляционных методов, то эти методы в целом используются в органической химии гораздо чаще по сравнению с неорганической. Первоначально корреляционные методы анализа были разработаны в рамках физической органической химии, они основаны на принципе линейных соотношений свободных энергий. Из упоминаемых в разд. Характерной особенностью комплексов с органическими лигандами является зависимость их устойчивости от числа членов металлсодержащего цикла. Для оценки относительной устойчивости комплексов рекомендуется также гипотеза аналогий, которая утверждает, что имеется соответствие между областью рН образования комплексов с монодентатными лигандами и комплексами с органическими реагентами с теми же донорными атомами. [28]
При изучении распределения алюминия концентрация металла в исходном и равновесном растворах определялась колориметрически по реакции с алюминоном. Сорбция проводилась из растворов ОД - 5 М хлорной кислоты, когда образование нерастворимых фосфатов полностью исключается. Такое сходство ряда избирательности с рядом относительной устойчивости ортофосфатных комплексов независимо от степени поперечной связанности сорбентов показывает, что сорбционные свойства циркокилфосфата тесно связаны с тенденцией металла к комплексообразованию с НгРО - группами, входящими в его состав; Таким образом, из всей гаммы факторов лияю-щих на избирательные свойства lifP для трехвалентных металлов, решающей является способность металла к комплексообразованию с фосфатными лигандами. [29]
Страницы: 1 2