Изофермент
Cтраница 3
Электрофоретическими методами установлено наличие 4 изоферментов церулоплазмина. В сыворотке новорожденных также были выявлены 2 фракции, имеющие большую электрофоре-тическую подвижность, чем изоферменты церулоплазмина взрослого человека. Следует отметить, что по своей электрофоретической подвижности изоферментный спектр церулоплазмина в сыворотке крови при болезни Вильсона-Коновалова сходен с изоферментным спектром новорожденных. [31]
Наиболее существенные отличия физико-химических свойств таких изоферментов определяются различием их аминокислотного состава ( табл. 16.2) и последовательности аминокислот. Например, для изоферментов человека наблюдается значительная разница в уровне активности. При гидратации С02 карбоангидраза В проявляет удельную активность около 40000 ед. С физиологической точки зрения интересно, что содержание этих изоферментов в организме неодинаково - - количество высокоактивной карбоангидразы С в 5 - 10 раз меньше, чем фермента типа В. Результатом этого является примерно равное распределение суммарной карбоангидразной активности между двумя изоферментами. [32]
 |
Электрофоретическая картина изоферментов ацетилхолин-эстеразы. содержащихся в головном мозгу радужной форели, акклимированной к различным температурам ( по данным Болдуина и Хочачки, 1970. [33] |
Клетки могут постоянно содержать смешанный набор изоферментов, включающий варианты, специфически приспособленные для работы в определенных диапазонах температур. При этом возможны сезонные сдвиги в количественном соотношении этих вариантов. [34]
Организм может включать и выключать синтез сезонных изоферментов, так что клетки особей, акклимированных к зимним и к летним условиям, содержат качественно различные наборы изоферментов. [35]
Карбоангидраза существует в нескольких молекулярных формах ( изоферменты А, В и С), которые можно разделить при помощи электрофореза. [36]
У радужной форели к ферментам, не имеющим сезонных изоферментов, относятся лактат-дегидрогеназа ( рис. 85) и малатдегидрогеназа. У обоих этих ферментов / См сравнительно мало изменяется в характерной для биологических систем области температур и отрицательная температурная модуляция отсутствует. [37]
При выделении ферментов иногда получают их различные формы ( изоферменты), обладающие одинаковой активностью, но характеризующиеся разными электрофоретическими и хромато-графическими свойствами. Как следует из приведенных далее примеров, это различие может быть вызвано несколькими причинами. [38]
Недавно Энтиан и соавторы описали разделение методом хроматофокусирования трех изоферментов энолазы из дрожжей. Все они являются гидрофобными белками. [39]
У полиплоидов появляются еще большие возможности для увеличения разнообразия изоферментов и дополнительные возможности для варьирования соотношения аллелей. [40]
В клетках различных млекопитающих креатинкиназа присутствует в виде трех цитоплазматических изоферментов ( мышечного, мозгового-и митохондриального), а также в виде митохондриального изофер-мента. [41]
Остается выяснить, так ли обстоит дело и с другими изоферментами. [42]
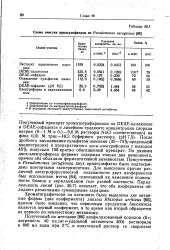 |
Схема очистки арнлсульфатазы из Pseudomonas aeruginosa [ Q3 ]. [43] |
Хроматографически на катионите были выделены две активные формы ( два изофермента) липазы Rhizopus arrhizus [65], причем было показано, что первичным продуктом биосинтеза является первый изофермент, в то время как второй образуется из первого по неизвестному механизму. [44]
Тонкая регулировка скоростей метаболических реакций, осуществляемая благодаря различной чувствительности изоферментов к аллостерическим модуляторам. Некоторые регуля-торные ферменты существуют в нескольких молекулярных формах, различающихся по своей чувствительности к модуляторам ( гл. [45]
Страницы: 1 2 3 4