Изохора
Cтраница 1
Изохора, соответствующая удельному объему УУКР, называется критической изохорой; она имеет общую касательную с линией насыщения в критической точке. [1]
Изохора и изобара реакции выражают количественную зависимость изменения подвижного равновесия химической реакции с изменением температуры в системе. Чтобы найти константы равновесия из уравнений ( 42 9) и ( 43 5), необходимо знать теплоты реакции как функции температуры Qv Qv ( T) и Qp Qp ( T) и значение константы равновесия при одной какой-либо температуре. [2]
Изохора, проходящая через эту точку, дает значение конечного удельного объема у2, необходимого для расчета выходного сечения сопла. [3]
 |
Изображение основных термодинамических процессов идеального газа в р, и-и Т, s - координатах. [4] |
Изохора ( п оо) делит поле диаграммы на две области: процессы, находящиеся правее изохоры, характеризуются положительной работой, так как сопровождаются расширением рабочего тела; для процессов, расположенных левее изохоры, характерна отрицательная работа. [5]
Изохора соответствует нагреванию или охлаждению тела при постоянном объеме, а изобара-при постоянном давлении. Поэтому они изображаются прямыми линиями, перпендикулярными к соответствующей оси. [6]
Изохора - единственный квазистатический процесс, в котором не совершается работа, все тепло идет на изменение внутренней энергии системы. [7]
Изохора для массы 2т газа составляет с осью абсцисс больший угол, чем изохора для массы m газа, причем tg р 2 tg се. [8]
Изохора на диаграмме s - i как в области влажного насыщенного пара, так и в области перегретого пара идет круче изобары. [9]
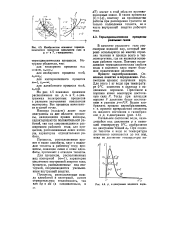 |
Изображение основных термодинамических процессов идеального газа в р, v - и 7, s - координатах. [10] |
Изохора ( п оо) делит поле диаграммы на две области: процессы, находящиеся правее изохоры, характеризуются положительной работой, так как сопровождаются расширением рабочего тела; для процессов, расположенных левее изохоры, характерна отрицательная работа. [11]
Изохорой, изобарой, изотермой, адиабатой и политропой называются линии, изображающие в какой-либо термодинамической диаграмме соответственно изо-хорный, изобарный, изотермический, адиабатный и поли-тропный процессы. [12]
 |
Изохорный и изобарный [ IMAGE ] - 4. Изотермный и адиабат-процессы в Гз-диаграмме ный процессы в Гз-диаграмме. [13] |
Как изохора, так и изобара в Гз-диаграмме строятся по нескольким точкам, координаты которых находятся вычислением. [14]
Уравнения изохоры и изобары химической реакции имеют большое практическое значение для расчета равновесий в системах при различных температурах, если известен тепловой эффект реакции. Наоборот, если известна зависимость константы равновесия от температуры, то можно вычислить тепловой эффект реакции. [15]
Страницы: 1 2 3 4