Изохора
Cтраница 2
Уравнения изохоры и изобары реакции характеризуют изменение константы равновесия с температурой. Они определяют эту зависимость в дифференциальной форме. Для практических расчетов равновесия при различных температурах обычно необходимо бывает предварительно интегрировать их. [16]
Уравнения изохоры и изобары химической реакции, полученные в дифференциальной форме, могут быть проинтегрированы, что позволяет получить зависимость вида In / С / ( Т), которая позволит определить константу равновесия при любых заданных температурах. [17]
Уравнения изохоры и изобары реакции характеризуют изменение константы равновесия с температурой. Они определяют эту зависимость в дифференциальной форме. Для практических расчетов равновесия при различных температурах обычно необходимо бывает предварительно интегрировать их. [18]
Уравнения изохоры и изобары реакции позволяют производить количественные расчеты изменения константы равновесия при изменении температуры, если известна величина теплового эффекта реакции. Эти уравнения используются также для расчета теплового эффекта реакции по известной величине константы равновесия. Для получения расчетных формул необходимо уравнения ( VII, 11) и ( VII, 12) проинтегрировать. Интегрирование особенно просто в предположении, что тепловой эффект не зависит от температуры. Это предположение может быть принято без особых погрешностей для небольших интервалов температуры, пренебрегая небольшими температурными изменениями теплового эффекта. [19]
Уравнения изохоры и изобары реакции характеризуют изменение константы равновесия с температурой. Они определяют эту зависимость в дифференциальной форме. Для практических расчетов равновесия при различных температурах обычно необходимо бывает предварительно интегрировать их. [20]
Уравнения изохоры и изобары реакции характеризуют изменение константы равновесия с температурой. Они определяют эту зависимость в дифференциальной форме. Для практических расчетов равновесия при различных температурах требуется интегрирование этих уравнений. [21]
Уравнения изохоры и изобары химической реакции позволяют количественно охарактеризовать смещение равновесий, в то время как принцип Ле-Шателье дает только качественную характеристику сдвига. [22]
Уравнения изохоры и изобары реакции характеризуют изменение константы равновесия с температурой. [23]
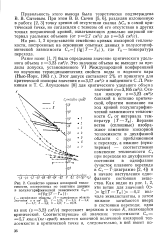 |
Семейство кривых изохорной теплоемкости, построенных по опытным данным в полулогарифмической зависимости С. [24] |
Считая изохору и3 23 см3 / г с мал / ( кг-гра Ю близкой к истинно критической, обратим внимание на ход кривой полулогарифмической зависимости теплоемкости Cv от интервала температур Т - ТП. Верхние ветви ( сплошные) изображают изменение изохорной теплоемкости в двухфазной области с приближением к переходу, а нижние ( пунктирные) - соответственно изменение теплоемкости Cv при переходе из двухфазного состояния в однофазное ( участок плавного перехода в Cv - Г - диаграмме [2, 4]) и в начале наступления однофазного состояния вещества. Как видно из рис. 1, 2, эти ветви для значений 0 g T - Тп - 0 2 вначале эквидистантны, а затем нижние загибаются вверх в состоянии перехода; одна из них ( v3 23 см3 / г) пересекает верхнюю в точке К, являющейся критической. [25]
По изохоре 2 - 3 подводится теплота q ( изображаемая пл. [26]
По постоянной изохоре 50 м3 / кмоль идем до пересечения с изобарой 1 ат; в точке пересечения находим изотерму 313 С. [27]
 |
Результаты исследования теплоемкости, воды в ся - 1 и е - lg ( Г - Тп-диаграммах ( слева от критической точки. [28] |
На критической изохоре переход теплоемкости с из двухфаз-нгго состояния в однофазное происходит плавно, с характерным закруглением. Полный переход в однофазное состояние совершается в некотором температурном интервале, в несколько раз превышающем величину температурного интервала, в котором был получен скачок Де при переходе пограничной кривой вдали от критической точки. Эту область состояния, весьма подвижную с термодинамической точки зрения, мы называем переходной ( критической) областью; конец этого состояния служит началомза-критической области. [29]
На изохорах вблизи линии [ насыщения существует предпереход-ная область, в которой происходит перемена знака температурной зависимости скорости и коэффициента поглощения. Эта предпереходная область наиболее отчетливо проявляется при больших плотностях. [30]
Страницы: 1 2 3 4