Адсорбция - данный компонент
Cтраница 2
Это - уравнение парциальной изотермы адсорбции, поскольку оно связывает равновесные величины адсорбции данного компонента с его равновесной концентрацией. [16]
Показано, что возможно подсчитать количества угля, необходимого для выделения из смесей различного состава при различных давлениях более тяжелого компонента, пользуясь изотермой адсорбции данного компонента и его парциальным давлением в смеси. [17]
Для расчета количества угля, необходимого для выделения других компонентов газа, входящих в смесь в различных соотношениях, была проверена возможность вычисления этого количества, пользуясь изотермой адсорбции данного компонента и его парциальным давлением в смеси. [18]
Чисто термодинамическое рассмотрение адсорбции из растворов не может послужить ни количественной, ни качественной основой селективности в жидкостной хроматографии, так как свойства компонентов растворов при таком рассмотрении остаются невыявленными. Энергия адсорбции данного компонента из жидкого раствора определяется разностью энергий межмолекулярного взаимодействия его молекул с адсорбентом и с соседними молекулами в конденсированном растворе. Поэтому часто она в несколько раз ( иногда на порядок) меньше энергии адсорбции того же компонента из газовой фазы. Это позволяет, во-первых, осуществлять жидкостно-адсорбци-онную хроматографию при значительно более низких температурах и, во-вторых, варьировать природу растворителя-элюента, добавляя к нему вещества, адсорбирующиеся сильнее или слабее данного компонента. В этом случае для полосы данного компонента имеет место адсорбция из трехкомпонентного раствора: данный компонент смеси, растворитель и добавленное к нему вещество, концентрация которого обычно много больше концентрации компонента разделяемой смеси. [19]
Применение для анализа растворов метода жидкостной хроматографии позволяет продвинуться в сторону малых концентраций равновесных растворов. Непосредственное определение адсорбции данного компонента из его хроматограммы, полученной на колонне с изучаемым адсорбентом при элюирова-нии изучаемым растворителем, рассмотрено в конце этой лекции. [20]
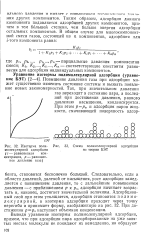 |
Изотерма полимолекулярной адсорбции ( с - равновесная концентрация, р - равновесное давление газа. [21] |
Таким образом, адсорбция данного компонента подавляется адсорбцией других компонентов, причем в тем большей степени, чем больше энергия адсорбции остальных компонентов. [22]
Таким образом, адсорбция данного компонента из бинарной газовой смеси увеличивается с повышением его парциального давления ( концентрации) и уменьшается с повышением парциального давления другого компонента. Адсорбция данного компонента подавляется адсорбцией другого и подавляется в тем большей степени, чем больше энергия адсорбции этого другого компонента. [23]
Адсорбция компонента / характеризуется кривой распределения его концентрации c / s по сечению поверхностного или межфазного слоя. Часто накапливающийся в поверхностном слое компонент входит в состав только одной фазы [ например, фазы ( J5) ] и не существует во второй фазе. В этом случае говорят об адсорбции данного компонента ( адсорбата) на поверхности второй фазы ( а) - адсорбента. В предельном случае все адсорбированные частицы вплотную прижаты к поверхности адсорбента, и кривая распределения имеет узкий и высокий максимум ( кривая 2), соответствующий положению частиц в первом слое от поверхности адсорбента. Этот предельный случай называют монослойной адсорбцией. При моно-слощюй адсорбции формальное значение концентрации c / s в адсорбционном слое велико и значение Г / практически совпадает с количеством вещества на единице площади / z / sVS, которое мы обозначим Л / и назовем реальной адсорбцией. [24]
Задача о фильтрации смеси веществ с учетом взаимодействия их со средой весьма сложна и в общем случае пока не решена. Трудность этой задачи может быть проиллюстрирована на примере, когда происходит адсорбция веществ. Если изотерма сорбции не линейна, то величина адсорбции данного компонента зависит от концентрации других компонентов смеси [ взаимозависимая сорбция - уравнение (3.8) ], Система уравнений материального баланса и кинетики сорбции, описывающих фильтрацию смеси, в этом случав настолько сложна, что аналитическое решение ее получить не удается. [25]
Изотерма гиббсовской адсорбции из трехкомпонентного раствора представляет собой поверхность, изобразить которую можно с помощью проекции линий одинаковой адсорбции на треугольник Гиббса. Принимая, что величина адсорбции между точками, сравнительно близко расположенными друг от друга, изменяется линейно, можно соединить каждую точку с ближайшей соседней и в середине отрезка определить значение адсорбции как среднее из величин адсорбции, измеренных в этих точках. Если таким же образом использовать и точки, лежащие на сторонах треугольника, которые выражают изотермы адсорбции данного компонента из двухкомпонентных растворов ( определение этих изотерм описано в гл. [26]
Страницы: 1 2