Адсорбция - пар - бензол
Cтраница 1
Адсорбция паров бензола и я-гек-сана на окиси и гидроокиси магния. [1]
При адсорбции пара бензола на непористой саже это относительное давление соответствует образованию сплошного мономолекулярного слоя. [2]
Величина адсорбции паров бензола на цеолите О значительно больше, чем для цеолита омега. В случае цеолита О повышение температуры обработки с 350 до 520 С значительно увеличивает сорбционную способность, а для цеолита омега наблюдается обратная зависимость. Для цеолита омега при повышенной температуре не исключена блокировка, особенно больших каналов, которые становятся только частично доступными для молекул бензола. [3]
Изотермы адсорбции паров бензола и к-гексана на окиси магния. [4]
При исследовании адсорбции паров бензола и фазовых переходов на цеолите NaX [43] удалось установить, что изостеры адсорбции состоят из двух линейных участков, соответствующих двум значениям теплот адсорбции при одном и том же заполнении. На этом основании принято допущение, что некоторые термодинамические свойства ( и, в частности, энтальпия) скачкообразно изменяются. При достаточно низких температурах и больших заполнениях бензол, адсорбированный в порах цеолита, может находиться в квазитвердом состоянии, когда его молекулы характеризуются только колебательными и вращательными степенями свободы. При повышении температуры ( при температурах изломов на изостерах) происходит размораживание трансляционных степеней свободы, и адсорбированный бензол переходит в квазижидкое состояние. Такое квазиплавление характерно для адсорбированного бензола, который из-за высокодисперсного состояния, своеобразного характера упаковки молекул в микропорах и других оеобенностей может по своим свойствам отличаться от свойств объемной фазы этого вещества. [5]
На изотерме адсорбции пара бензола ( см, рис. 153) взята произвольная точка с координатами: Ро-10 мм рт. ст., а0 0 262 кг / кг. [6]
При исследовании адсорбции паров бензола и фазовых переходов на цеолите NaX [43] удалось установить, что изостеры адсорбции состоят из двух линейных участков, соответствующих двум значениям теплот адсорбции при одном и том же заполнении. На этом основании принято допущение, что некоторые термодинамические свойства ( и, в частности, энтальпия) скачкообразно изменяются. При достаточно низких температурах и больших заполнениях бензол, адсорбированный в порах цеолита, может находиться в квазитвердом состоянии, когда его молекулы характеризуются только колебательными и вращательными степенями свободы. При повышении температуры ( при температурах изломов на изостерах) происходит размораживание трансляционных степеней свободы, и адсорбированный бензол переходит в квазижидкое состояние. Такое квазиплавление характерно для адсорбированного бензола, который из-за высокодисперсного состояния, своеобразного характера упаковки молекул в микропорах и других особенностей может по своим свойствам отличаться от свойств объемной фазы этого вещества. [7]
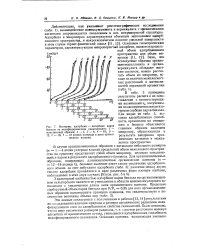 |
Изотермы адсорбции - десорбции паров бензола на модифицированном палыгорските. / - естественный образец. 2 - 1. 3 - 4. 4 - 10. 5 - 12. 6 - 16. 7 - 18 атомов углерода в цепи органического катиона. [8] |
Характерной особенностью адсорбции паров бензола на органозамещен-ном палыгорските является ее уменьшение в области мономолекулярного заполнения с увеличением длины цепи органического катиона. [9]
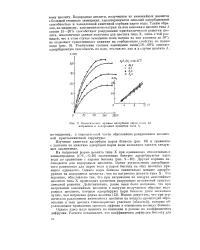 |
Кинетические кривые адсорбции паров воды на натриевом и водородных цеолитах типа X. [10] |
Изучение кинетики адсорбции паров бензола ( рис. 10) и сравнение с данными по кинетике адсорбции паров воды позволяют сделать следующее заключение. [11]
Полученные изотермы адсорбции паров бензола на исходных и виброизмельченных силикагелях хорошо описываются двучленным уравнением изотермы адсорбции теории объемного заполнения микропор. Параметры микропористой структуры исследованных силикагелей позволяют проследить за их изменением под влиянием виброизмельчения. [12]
На изотерме адсорбции пара бензола ( см. рис. 153) взята произвольная точка с координатами: РоЮ мм рт. ст., д0 0 262 кг / кг. [13]
Основное отличие изотерм адсорбции паров бензола на каолините от изотерм на монтмориллоните состоит в том, что на каолините адсорбция обратима при любой температуре. С ростом температуры максимальная величина адсорбции несколько увеличивается, что обусловлено удалением сорбированной воды. [14]
Теплота и энтропия адсорбции паров бензола и к-гексана на гидроокиси магния. [15]
Страницы: 1 2 3 4 5