Адсорбция - атомарный водород
Cтраница 2
Нами было показано, что на активированном угле при низких температурах ( 90 К) обмен между водородом и дейтерием и пара-орто-пре-вращение протекает с большой скоростью и с энергией активации, не превышающей 300 кал. В этих работах также было показано, что активированно-адсорбированный водород и адсорбция атомарного водорода отравляют поверхность угля по отношению к указанным реакциям. Исследование кинетики пара-орто-иревращения и обмена привело нас к выводу, что эти реакции протекают путем взаимодействия адсорбированной молекулы, в которой связь между атомами деформирована, с молекулой водорода из газовой фазы. Существование на поверхности угля деформированных молекул водорода было объяснено по Эйрингу и Шерману наличием на этой поверхности участков с определенным расстоянием между атомами углерода. Другое представление о механизме пара-орто-превращения и обмена, основанное на взаимодействии адсорбированного атома водорода с молекулой водорода из газовой фазы, требует дополнительного предположения, что время жизни адсорбированного атома меньше времени, нужного для взаимодействия этого атома с углем, так как уголь отравляется атомарным водородом. [16]
 |
Зависимость теплоты адсорбции водорода на никеле от степени покрытия подложки водородом. [17] |
Данные по адсорбции водорода указывают, что г и s - атомы являются двумя простейшими поверхностными комплексами. Эти элементарные комплексы играют, по-видимому, существенную роль не только при адсорбции атомарного водорода, но и во всех других случаях, когда адсорбент содержит водородные атомы: последнее относится, например, к адсорбции и каталитическим реакциям на металлической поверхности молекул водорода. Спектры ИК поглощения в области 6 - 8 мкм указывают, что на поверхности атомарный водород и дейтерий существуют в виде г и s - атомов. [18]
Механизм включения водорода в электроосажденные металлы может быть различным. Как уже отмечалось, один из путей попадания водорода в осадок может заключаться в адсорбции атомарного водорода на поверхности в процессе осаждения металла. Адсорбированный водород частично ре-комбинируется и удаляется в виде молекулярного водорода, а частично переходит в кристаллическую решетку металла, занимая узлы в кристаллической решетке или располагаясь между ними, и образует твердые растворы. При этом необходимо отметить, что образование твердых растворов между металлом и водородом при электроосаждении металла возможно также и вследствие непосредственного включения иона водорода в кристаллическую решетку в виде протона, в отличие от включения адсорбированных атомов. О возможности такого протонного включения водорода в электролитический металл свидетельствует экспериментальный факт большего наводороживания металла в кислых растворах по сравнению с щелочными. [19]
Если предположить, что изменение перенапряжения водорода при переходе от Pt к Hg целиком обусловлено изменением энергии адсорбции атомарного водорода, то получается Eng - u 27 ккал / моль. Таким образом, экспериментальные данные подтверждают основные положения теории замедленного разряда о влиянии материала электрода на скорость электрохимической реакции. [20]
Это снижение происходит как за счет меньшего захвата молекулярного водорода растущими гранями осадка, так и за счет уменьшения адсорбции атомарного водорода на катодной поверхности. Анализ скорости вакуумной экстракции водорода из осадков показал, что имеются значительные отличия в кинетике выделения газов из облученных осадков по сравнению с обычными. Из облученного образца основная масса водорода выделяется при температуре 500 С. Для полного удаления газа образец нужно прогревать в течение 30 мин. Для максимального удаления газа из обычного образца требуется гораздо более высокая температура и более длительный промежуток времени. Все это позволяет судить о том, что природа внедрения водорода в озвучиваемый осадок никеля имеет иной характер, а прочность связи металл-водород слабее. [21]
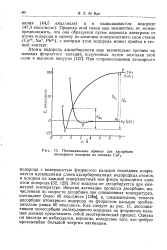 |
Потенциальные кривые для адсорбции атомарного водорода на пленках СаР2. [22] |
Этот водород не десорбируется при комнатной температуре. Энергия активации процесса десорбции, вычисленная по скорости десорбции при повышенных температурах, оставляет более 40 ккал / моль [ 128в ], а, следовательно, теплота адсорбции атомарного водорода на фтористом кальции приблизительно равна 60 ккал / моль. Как следует из рис. 15, диссоциативная хемосорбция молекулярного водорода на фтористом кальции должна представлять собой экзотермический процесс. Однако н никогда не наблюдался, вероятно, вследствие того, что требует чрезвычайно большой энергии активации. [23]
Этот водород не десорбируется при комнатной температуре. Энергия активации процесса десорбции, вычисленная по скорости десорбции при повышенных температурах, составляет более 40 ккал / моль [ 128в ], а, следовательно1, теплота адсорбции атомарного водорода на фтористом кальции приблизительно равна 60 ккал / моль. Как следует из рис. 15, диссоциативная хемосорбция молекулярного водорода на фтористом кальции должна представлять собой экзотермический процесс. Однако он никогда не наблюдался, вероятно, вследствие того, что требует - чрезвычайно большой энергии активации. [24]
Теплота адсорбции атомарного водорода на металлах составляет обычно 40 - 50 ккал. Теплота адсорбции атомарного водорода на А12О3 должна быть много меньше, порядка величины, найденной для стекла или кремнезема, которая оказалась заметно больше 5 ккал. [25]
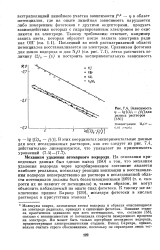 |
Зависимость Ф - lg [ ( 2 / 0 - / / / ] для разных растворов. [26] |
Молекулы спирта, захватывая атомы водорода и образуя окисляющиеся на электроде радикалы, приводят к снижению фототока. Влияние этанола практически одинаково при всех потенциалах, что, согласно [53], связано с независимостью от потенциала скорости замедленного процесса на электроде. Им может быть только адсорбция атомарного водорода, предшествующая электрохимическим стадиям. [27]
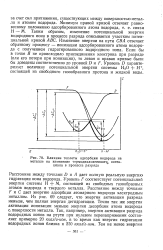 |
Влияние теплоты адсорбции водорода на металле на изменение термодинамического, потенциала в процессе разряда. [28] |
Расстояние между точками D и Л дает полную реальную энергию-гидратации иона водорода. Уровень F соответствует потенциальной энергии системы Н М, состоящей из свободных газообразных атомов водорода и твердого металла. Расстояние между точками F и С дает энергию адсорбции атомарного водорода электродным металлом. Из рис. 69 следует, что энергия активации разряда меньше, чем полная энергия дегидратации. Точно так же энергия активации ионизации меньше энергии десорбции атома водорода а поверхности металла. Так, например, энергия активации разряда водородных ионов на ртути при нулевом перенапряжении составляет примерно 20 ккал / г-ион, в то время как энергия гидратации водородных ионов близка к 250 ккал / г-ион. [29]
Заметное влияние на структуру осадков оказывает растворение в них водорода. Механизм включения водорода в осадок может быть различным. Один из путей попадания водорода в осадок может заключаться в адсорбции атомарного водорода на поверхности в процессе осаждения металла. Адсорбированный водород частично рекомбинируется и превращается в молекулярный водород, а частично переходит в кристаллическую решетку металла, занимая узлы в ней или располагаясь между ними, и образует твердые растворы; возможно также и непосредственное включение иона водорода в кристаллическую решетку в виде протона. [30]
Страницы: 1 2 3