Адсорбция - чужеродная частица
Cтраница 1
 |
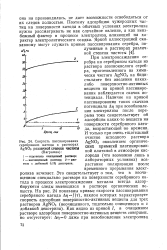
Зависимость скорости выделения молибдена ( 1, никеля ( 2 и водорода ( 3 от концентрации Na2MoO4 при совместном восстановления молибдена и никеля из лимонноаммиачно-го электролита ( ф - 1200 мв. [1] |
Адсорбция чужеродных частиц при восстановлении ионов металла как правило, приводит к повышению поляризации. Так, например, восстановление хромат-ионов из растворов хромовой кислоты на окисленной поверхности хрома настолько затруднено, что практически происходит лишь разряд ионов водорода, несмотря на то что потенциал восстановления ионов водорода намного отрицательней, чем хромат-иона. [2]
 |
Скорость пассивирования серебряного катода в растворах AgN03 различной степени чистоты ( Ваграмян. [3] |
Поэтому адсорбцию чужеродных частиц на поверхности катода в обычных условиях электролиза нужно рассматривать не как случайное явление, а как неизбежный фактор в процессе электролиза, влияющий на характер электролитического осадка. [4]
Из приведенных данных видно, что в результате адсорбции чужеродных частиц состояние поверхности электрода изменяется, что и определяет число возникающих кристаллов, причем величина поляризации в этом случае сама является функцией состояния поверхности катода. [5]
Однако следует учитывать, что в процессе совместного восстановления ионов металлов изменяется не только природа подкладки, но может изменяться и состояние поверхности электрода за счет адсорбции чужеродных частиц. [6]
Когда скорость адсорбции мала, наблюдается конкуренция двух противоположно направленных процессов: осаждение металла и увеличение активной поверхности, с одной стороны, и пассивирование поверхности вследствие адсорбции чужеродных частиц и уменьшение активной части электрода - с другой. В результате этих процессов на участках, где происходит замедление выделения металла, пассивирование превалирует над осаждением, и металл перестает выделяться. Участки же, где сохраняется высокая скорость осаждения металла, остаются активными и продолжают расти. Вследствие роста одних участков поверхности и прекращения осаждения металла на других осадок металла получается неравномерным. [7]
Можно предполагать, что изменение скорости обмена от способа подготовки поверхности металла связано не только с изменением величины истинной поверхности, но и с изменением кристаллографической активности и структуры металла, а также с адсорбцией чужеродных частиц и образованием поверхностных соединений. [8]
Это может быть связано с тем, что при повышении температуры уменьшается необратимая адсорбция чужеродных частиц и увеличивается скорость растворения или разрушения пассивных слоев, образующихся в растворе на поверхности металлов. Поскольку степень адсорбции чужеродных частиц на поверхности электродов, связанная с реакционной способностью металлов группы железа по отношению к среде, различна у никеля, кобальта и железа, то и условия обратимости электродов достигаются при различных температурах. [9]
Преобладание процесса возникновения новых зародышей над скоростью роста уже имеющихся кристаллов особенно характерно для комплексных электролитов, а также для растворов простых солей, содержащих ПАВ. В последнем случае из-за адсорбции чужеродных частиц на растущих гранях линейная скорость роста кристаллов уменьшается и осадки получаются высокодисперсными. Весьма часто при этом они не имеют даже четко выраженной кристаллической структуры. При обратном соотношении скоростей, когда линейная скорость роста кристаллов начинает преобладать, осадок имеет грубую кристаллическую структуру. В общем случае образованию мелкокристаллических осадков способствует: повышение плотности тока на катоде, понижение температуры электролита, добавки нейтральных солей ( снижающих концентрацию ионов осаждаемого металла у катода), разбавление раствора, введение в электролит ПАВ, ком-плексообразование. [10]
Металлы 2 - й группы, восстанавливающиеся с высоким перенапряжением ( Fe, Co, Ni, Сг, Мп и др.), склонны к пассивированию. Существование на катоде такой пленки вследчвие адсорбции чужеродных частиц повышает перенапряжение и позволяет осаждать такие металлы нз некоторых их солей. Для чгих металлов характерна повышенная реакционная способность по отношению к среде и образование поверхностных соединений. Они выделяются на катоде в виде тонкого слоя окиси inn ( идроокиси. [11]
Металлы 2 - й группы, восстанавливающиеся с высоким перенапряжением ( Fe, Co, Ni, Ст, Ми п др.), склонны к пассив. Существование на катоде такой пленки вследствие адсорбции чужеродных частиц повышает перенапряжение и позволяет осаждать такие металлы из некоторых их солей. Для чгих металлов характерна повышенная реакционная способность по отношению к среде и образование поверхностных соединений. Они выделяются на катоде Е виде тонкого слоя окиси inn ждроокнси. [12]
Металлы 2 - й группы, восстанавливающиеся с высоким перенапряжением ( Fe, Co, Ni, Cr, Мп и др.), склонны к пассивированию. Существование на катоде такой пленки вследствие адсорбции чужеродных частиц повышает перенапряжение и позволяет осаждать такие металлы из некоторых их солей. Для этих металлов характерна повышенная реакционная способность по отношению к среде и образование поверхностных соединений. Они выделяются на катоде в виде тонкого слоя окиси или гидроокиси. [13]
Существование на катоде такой пленки вследствие адсорбции чужеродных частиц повышает перенапряжение и позволяет осаждать такие металлы из некоторых их солей. [14]
Изменение соотношения скоростей разряда ионов кобальта и никеля при их совместном осаждении ( см. рис. 74 и 76) объясняется уменьшением ингибирующего действия чужеродных частиц с повышением температуры. Если исходить из того, что степень адсорбции чужеродных частиц на сплаве является промежуточной по сравнению с адсорбцией на отдельных металлах, то разряд ионов кобальта на сплаве должен происходить с меньшей скоростью, чем на кобальте, а разряд ионов никеля на сплаве - с большей скоростью, чем на никеле. [15]
Страницы: 1 2