Адсорбция - другой газ
Cтраница 1
Адсорбция других газов на металлических пленках также приводит к определенному значению потенциала. Так, углекислый газ адсорбируется при значении потенциала около - 500 мв против воздушно-серебряного электрода сравнения. Адсорбированный углекислый газ легко вытесняется с поверхности водородом, и при этом устанавливается обычный водородный потенциал. [1]
Однако адсорбция других газов ( азота и аргона) происходит иначе. Максимум адсорбции азота достигается при - 120 С, аргона при - 150 С. При очень низких температурах ( - 190 С и ниже) адсорбция азота и аргона становится совсем незначительной по сравнению с ее максимальным значением. [2]
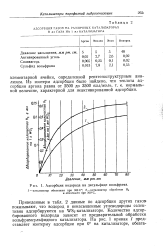 |
Адсорбция водорода на дисульфиде вольфрама. [3] |
Приведенные в табл. 2 данные по адсорбции других газов показывают, что водород и ненасыщенные углеводороды селективно адсорбируются на ШЗа-катализаторе. Количество адсорбированного водорода зависит от предварительной обработки вольфрамсульфидного катализатора. [4]
Наличие хорошей корреляции теплоты образования оксида с теплотой адсорбции других газов, кроме кислорода, имеет глубокий смысл. При сопоставлении каталитической активности металлов в разложении NH3 на N2 и Н2 и в обратной реакции синтеза NH3 с теплотами образования оксидов этих элементов получается график с экстремумом, подобный приведенному на рис. 5.7. У Re и Pt с большой и низкой теплотами образования оксидов соответственно каталитическая активность невелика, у Ru она промежуточная, а Со и Fe с промежуточной теплотой образования оксидов имеют высокую каталитическую активность. Установление подобных зависимостей каталитической активности от некоторых доминирующих свойств элементов полезно для разработки катализаторов. [5]
Потенциальная теория не дает возможности удовлетворительно рассчитать адсорбцию одного газа, исходя из данных по адсорбции другого газа; однако она, как мы видели, прекрасно передает температурную зависимость изотерм адсорбции. Поэтому представляет большой интерес сравнить наклоны кривых эквивалентных давлений одного и того же газа при различных температурах, вычисленные как на основании теории капиллярной конденсации, так и потенциальной теории. [6]
Из-за большого разброса экспериментальных данных по адсорбции азота на активных углях очень трудно указать надежные относительные данные по адсорбции других газов путем сравнения различных результатов, особенно полученных на неидентичных адсорбентах. [7]
На полимеризацию указывает превышение адсорбции данного-газа по сравнению с соответствующей монослойному покрытию поверхности, как это было установлено на адсорбции других газов. [8]
Это показано на рис. 3 на примере адсорбции этана при 100 С. Адсорбция других газов на отработанном и неактивном АМ - катализаторе уменьшается в еще большей степени. [9]
Это показано на рис. 3 на примере адсорбции этана при 100 С. Адсорбция других газов на отработанном и неактивном Ш82 - катализаторе уменьшается в еще большей степени. [10]
Мы приводим здесь лишь немного примеров и для подробного ознакомления с обсуждаемым вопросом рекомендуем читателю литературу, упомянутую в начале данного раздела. Отметим лишь, что при адсорбции других газов на металлах они ведут себя аналогично водороду. [11]
На изотерме адсорбции чистой S02 имеется широкая петля гистерезиса, в то время как адсорбция других газов полностью обратима. Изотермы адсорбции азота и двуокиси углерода описываются уравнением Фрейндлиха, а изотерма адсорбции S02 - уравнением Ленгмюра. Применив эти уравнения, удалось найти корреляцию между изотермами адсорбции смесей и отдельных компонентов. [12]
Из ( 23 6 1), в частности, следует, что если 6 и 6 отличны от нуля, а одна из производных левой части равна нулю, то и другая производная тоже должна равняться нулю. А это означает, что если при конечных плотностях газов плотность адсорбции одного из них достигает экстремума, то плотности адсорбции других газов тоже должны достичь экстремума. [13]
Было показано, что, действительно, метод точек В может быть применен для измерений величины поверхности катализаторов при изучении адсорбции вышеперечисленных газов, если только измерения проводятся при температурах, близких к точкам кипения соответствующих газов. Однако аналогичные опыты с адсорбцией бутана показали, что для многих изотерм метод точки В неприменим. На этом же рисунке приведены изотермы адсорбции других газов. Ясно, что на такой изотерме, как изотерма адсорбции бутана, которая на всем своем протяжении весьма близка к прямой линии, почти невозможно выбрать точку В. [14]
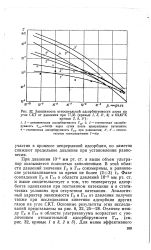 |
Зависимость относительной адсорбируемости азота на угле СКТ от давления при 77 35 ( кривые /, 3, 3, 4 и 63 45 К. [15] |
Страницы: 1 2