Адсорбция - другой газ
Cтраница 2
При давлении 10 - 5 мм рт. ст. и выше объем ультра-пор оказывается полностью заполненным. Факт совпадения Гд и Гст в области давлений ICh5 мм рт. ст. и выше свидетельствует о том, что температура адсорбента одинаковая при постоянном натекании и в статических условиях при отсутствии натекания. Аналогичный характер зависимости Тд и Гст от давления получен также при исследовании кинетики адсорбции других газов на угле СКТ. [16]
Найдено, что экстинкция полосы поглощения азота несколько изменяется в зависимости от способа обработки образца. Поэтому в табл. 1 приведено максимальное число центров В ъ на 1 г и на 1 см Ni, определенное на образцах разных типов. Экстинкция полосы поглощения азота при 20 см рт. ст. и при комнатной температуре, измеренная до адсорбции других газов, показана длиной стрелки на всех соответствующих рисунках. [17]
В первой статье Применение магнитных методов к хемосорбции и гетерогенному катализу излагаются физические основы и результаты нового магнитного метода. Селвудом метод интересен тем, что позволяет следить за изменением магнитных свойств катализатора во время реакции. В статье подробно описаны результаты исследования поведения водорода на никеле; кроме того, сообщаются данные для адсорбции других газов и паров, начиная от гелия и аргона и кончая бензолом и циклогексаном. На основании подобного рода магнитных измерений получены ценные сведения о механизме ряда каталитических реакций. [18]
Подобно этому газ 1 уменьшает адсорбцию газа 2 соответственно его парциальному давлению и адсорбционному коэффициенту рг и &. Из уравнений ( 5) и ( 6) следует, что один газ всегда уменьшает адсорбцию другого. Повышение адсорбции другого газа не может быть объяснено на основе теории Лэнгмюра. [19]
Химическая и кристаллографическая структуры различных кристаллических плоскостей одного и того же кристалла могут значительно различаться, поэтому следует изучать химические свойства кристалла в зависимости от вида экспонируемой грани. Такие исследования начались с известных экспериментов Гуотми и сотрудников, показавших, что монокристаллы меди и никеля реагируют с газами по-разному, в зависимости от вида грани, выходящей на поверхность. На рис. 2.16 приведены данные по адсорбции азота на монокристалле вольфрама, которые убедительно доказывают, что вероятность адсорбции, характер процесса и равновесное состояние для различных кристаллических граней значительно отличаются друг от друга. Наименее активна грань ( ПО), причем активность ее остается низкой и при адсорбции других газов, например водорода. Объясняется это тем, ято грань ( 110) имеет максимальную плотность атомов на поверхности и, как следствие, минимальную поверхностную энергию и высокую химическую стабильность. В некоторых случаях картина более сложна: например, при перестройке плоскости ( 100) структура ( 1 х 1) переходит в ( 1 х 5) или ( 5 х 20), адсорбционная способность которых значительно ниже. [20]
Отсутствие повышения скорости в таких опытах с добавками твердого продукта, возможно, по крайней мере частично объясняется указанной недостаточностью контакта между на - меренно добавленным твердым продуктом и исходным веществом. С целью выяснения степени контакта нами с В. А. Протащиком [ 131 были поставлены опыты по изотопному обмену между формиатом кобальта и металлическим кобальтом. Результаты этих опытов показывают на отсутствие изотопного обмена в этой системе; этот результат согласуется с представлением о недостаточности контакта между заранее внесенным твердым продуктом и исходным веществом. Причиной отсутствия каталитического действия в таких опытах могут быть, однако, также отличия в свойствах поверхности твердого продукта, образующегося in situ, и продукта, на котором произошла адсорбция атмосферных и других газов при перенесении его из реакционной трубки и смешении со свежей порцией исходного вещества. [22]
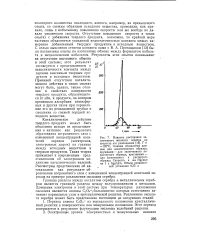
Для того чтобы эти явления изучить в простой системе газ - поверхность, были сняты изотермы адсорбции азота при 78 1, 83 5 и 89 2 К на монокристаллических и поликристаллических поверхностях меди [73]; при этом применялась прецизионная дифференциальная микрогравиметрическая методика. Площади всех поверхностей определялись согласно описанному выше методу Брунауэра - Эм-метта - Теллера. На рис. 29 показана изотерма адсорбции азота на ромбоэдрической грани кристалла меди во всем интервале давлений вплоть до 1500 мм рт. ст. В общих чертах форма этой кривой является типичной для изотерм адсорбции других газов, например аргона, как на других кристаллических гранях меди, так и на гранях кристаллов цинка и железа. Адсорбция азота и аргона на поверхностях монокристаллов всех трех металлов изучалась в температурном интервале 78 - 90 К с применением микровесов. Для облегчения расчета изостерических теплот адсорбции на рис. 29 представлена зависимость количества адсорбированного вещества от давления. [23]
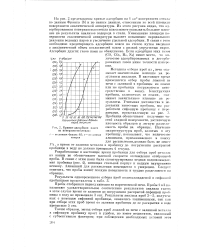 |
Кривые адсорбции влаги па поверхности стекла. [24] |
На рис. 2 представлены кривые адсорбции на 1 см поверхности стекла по данным Франка [6] и по нашим данным, отнесенным ко всей площади поверхности аналитической аппаратуры. Из этого рисунка видно, что адсорбированная поверхностью стекла влага может оказывать большое влияние на результаты анализов водорода в стали. В связи с этим необходимо предотвращать адсорбцию влаги на стекло путем введения в аналитически объем поглотителей влаги с низкой упругостью паров. Адсорбции других газов нами не обнаружено. [25]
Газ 2 уменьшает адсорбцию газа 1 тем больше, чем больше рг и Ь2 т - е - его парциальное давление и коэффициент адсорбции. Подобно этому газ 1 уменьшает адсорбцию газа 2 соответственно его парциальному давлению и адсорбционному коэффициенту рг и Ьг. Из уравнений ( 5) и ( 6) следует, что один газ всегда уменьшает адсорбцию другого. Повышение адсорбции другого газа не может быть объяснено на основе теории Лэнгмюра. [26]
Страницы: 1 2