Возможность - диссоциация
Cтраница 1
Возможность диссоциации этих гидроокисей по обоим направлениям обусловливает их химическое взаимодействие с кислотами и щелочами. При действии на соответствующую систему сильной кислотой последняя подавляет диссоциацию гидроокиси по кислотному типу и одновременно связывает ионы ОН основания в практически недиссоциированные молекулы воды. [1]
Возможность диссоциации этих гидроокисей по обоим направлениям обусловливает их химическое взаимодействие с кислотами и щелочами. При действии на соответствующую систему сильной кислотой последняя подавляет диссоциацию гидроокиси по кислотному типу и одновременно связывает ионы ОН7 основания в практически недиссоциированные молекулы воды. [2]
Возможность диссоциации этих гидроокисей по обоим направлениям обусловливает их химическое взаимодействие с кислотами и щелочами. При действии на соответствующую систему сильной: кислотой последняя подавляет диссоциацию гидроокиси по кислотному типу и одновременно связывает ионы ОН основания в практически недиссоциированные молекулы воды. [3]
Возможность диссоциации этих гидроокисей по обоим направлениям обусловливает их химическое взаимодействие с кислотами и щелочами. При действии на соответствующую систему сильной кислотой последняя подавляет диссоциацию гидроокиси по кислотному типу и одновременно связывает ионы ОН основания в практически недиссоциированные молекулы воды. [4]
Возможность диссоциации молекул на ионы в растворах в соединении с довольно большой химической активностью ионов обусловливает легкость протекания ионных реакций в растворах. Поэтому ионные реакции в растворах широко распространены и для жидкой среды являются наиболее распространенным типом химического превращения. [5]
Возможность диссоциации винтовой дислокации на частичные, расположенные в металлах с о. В этом случае высокое сопротивление движению дислокаций обусловлено необходимостью стягивания расщепленной дислокации с последующей рекомбинацией и образованием перетяжек, способных скользить в кристаллической решетке, поскольку эти процессы связаны со значительным увеличением энергии дислокации. Модель диссоциации и рекомбинации винтовых дислокаций удовлетворительно объясняет температурную зависимость сопротивления кристаллической решетки движению дислокации, высокий уровень напряжения течения при О К для о. Атомы внедрения могут стабилизировать сидячую дислокационную конфигурацию и понижать вероятность образования перетяжки на расщепленной дислокации, что приводит к возрастанию напряжения Пайерлса при увеличении концентрации примесей внедрения. [6]
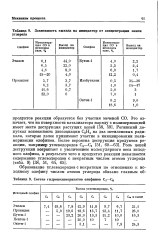 |
Зависимость выхода на инициатор от концентрации окиси углерода.| Состав гидрополимеризатов олефинов С2 - С8. [7] |
Рогинский допускал возможность диссоциации С2Н4 на два метиленовых радикала, которые далее принимают участие в инициировании полимеризации олефинов. [8]
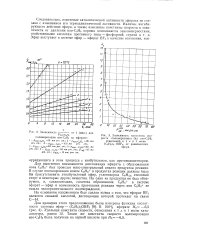 |
Зависимость константы скорости полимеризации ( ki изо - С4Нв, отнесенной к 1 л и 1 молю ОВРз, от равновесного эфира. [9] |
Для выяснения возможности диссоциации эфирата с образованием иона С2Н5 был проведен масс-спектральный анализ продуктов реакции. В случае инициирования ионом С2Н5 в продуктах реакции должны были бы присутствовать этилбутиловый эфир, углеводород C6Hi2, этиловый спирт и некоторые другие вещества. Ни один из продуктов не был обнаружен, и, следовательно, гипотеза образования C2Hs в системе эфират - эфир и возможность протекания реакции через ион С2Н5 не нашли экспериментального подтверждения. [10]
Мы исключаем лишь возможность диссоциации в адсорбированном слое. [11]
Таким образом, возможность диссоциации сильного электролита зависит от соотношения между силой, удерживающей ионы в кристаллической решетке, и силами взаимодействия их с растворителем. Растворение происходит тогда, когда сумма величин Uc больше или близка к энергии UKp. Например, энергия кристаллической решетки хлористого натрия i / NaCi 185 0 ккал, а величины Uc в воде имеют следующие значения: натрия 101 0 ккал, хлора-84 ккал. Их сумма равна 185 ккал. [12]
Таким образом, возможность диссоциации молекулы газа ударом быстрого иона при применявшихся энергиях ионов щелочных элементов нельзя считать экспериментально доказанной. Вместе с тем диссоциация молекулярных ионов при их столкновениях с молекулами газа при достаточно большой энергии ионов представляет собой твердо установленный факт. Отсюда можно заключить, что для диссоциации молекул ударом быстрого иона требуются значительно большие энергии ионов, чем те, которые применялись в опытах А. Б. Шехтер и сотрудников. [13]
Таким образом, возможность диссоциации сильного электролита решается соотношением между силой, удерживающей ионы в кристаллической решетке, и силами взаимодействия их с растворителем. Растворение происходит тогда, когда сумма величин Ах больше или близка к энергии UQ. [14]
Наиболее интересна для химика возможность диссоциации, являющейся результатом возбуждения электронами колебательных уровней. Электроны могут последовательно возбуждать все более высокие колебания. Было бы желательно ответить на вопрос, какова вероятность такой диссоциации в практически важных системах. В большинстве реальных систем наиболее вероятна, видимо, диссоциация при электронном ударе, идущая через возбуждение электронного уровня. [15]
Страницы: 1 2 3 4