Возможность - изоморфное замещение
Cтраница 2
Диагональная аналогия, обусловленная изоморфным замещением элементов, распространена значительно шире. Так как возможность изоморфного замещения объясняется преимущественно размерным фактором, особенно при замещении катионообразователей, то причиной этого вида диагональной аналогии является лишь малое различие атомных радиусов. Так, можно отметить близость орбитальных радиусов в диагональной паре Na - Ca, что проявляется в широком изоморфизме этих элементов в силикатных и сложных оксидных системах. В то же время о глубокой химической аналогии между ними говорить нельзя, так как их силовые характеристики сильно различаются. [16]
 |
Зависимость электроотрицательности ( я и орбитальных радиусов ( б элементов 2-го и 3-го периодов от порядкового номера. [17] |
Диагональная аналогия, обусловленная изоморфным замещением элементов, распространена значи гельно шире. Так как возможность изоморфного замещения объясняется преимущественно размерным фактором, особенно при замещении катионообразователей, то причиной этого вида диагональной аналогии является лишь малое различие атомных радиусов. Так, можно отметить близость орбитальных радиусов в диагональной паре Na - Ca, что проявляется в широком изоморфизме этих элементов в силикатных и сложных оксидных системах. В то же время о глубокой химической аналогии между ними говорить нельзя, так как их силовые характеристики сильно различаются. [18]
Это положение иллюстрирует разницу между типом связи в этих двух классах соединений. В ионных окислах возможность изоморфного замещения определяется главным образом размерами ионов, так как рассматриваемые ионы должны занимать пустоту определенного размера ( например, между четырьмя или шестью ионами О2 -) в решетке ионов кислорода, которые обычно находятся в плотной ( или в почти плотной) упаковке. Химические свойства ионов играют меньшую роль. Таким образом, следующие ионы могут замещать друг друга в структурах окислов: Fe2, Mg2, Mn2, Zn2 в окта-эдрическнх положениях, и ион Na значительно чаще замещает Са2 ( который имеет такой же ионный радиус), чем К, более близкий к первому по химическим свойствам. С другой стороны, в сульфидах критерием является образование одинакового числа связей, и такие атомы, как медь, железо, молибден, олово, серебро и ртуть, замещают цинк в цинковой обманке или в близких к ней соединениях. Элементы мышьяк и сурьма могут замещать серу по причинам, которые изложены ниже. В кристаллах, обладающих изоморфным замещением, проявляется беспорядочное распределение различных атомов металла по соответствующим положениям. Однако в структурах, которые мы сейчас рассмотрим, различные сорта атомов расположены регулярно, и осложнения, вызываемые замещением, можно устранить при изучении веществ с составом, приближающимся к идеальному. [19]
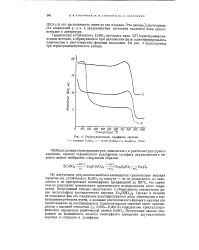 |
Термогравиграммы сульфатов европия. [20] |
Из полученных результатов наиболее неожиданна сравнительно высокая термическая устойчивость EuSO4 на воздухе - он не разлагается, не окисляется и не претерпевает полиморфных превращений до 550 С, что значительно расширяет возможности практического использования этого соединения. Однако в отличие от остальных фаз это соединение идентифицируется лишь химическим и термогравиметрическим путем, а данными рентгеновского фазового анализа его существование не подтверждается. Полученные данные указывают на возможность полного изоморфного замещения двухвалентного европия и стронция в сульфатах. [21]
Постоянным спутником лантанидов в природе является иттрий. Этот элемент, строго говоря, не входящий в группу редкоземельных, в результате явления лантанидной контракции по ряду свойств ( величина ионного радиуса, основность, растворимость солей) занимает определенное место в иттриевой подгруппе. Как известно, величина ионного радиуса является одним из основных факторов возможности изоморфного замещения. [22]
Если принять во внимание, что энергетические и силовые характеристики атомов в основном определяют их химический облик, а размерный фактор регламентирует взаимодействие низшего порядка, например образование твердых растворов, то становится понятной диагональная аналогия в широком смысле. Отметим, что она возможна только для элементов начала малых периодов и не наблюдается как при переходе к более тяжелым групповым аналогам, так и при дальнейшем продвижении по периодам вправо. Диагональная аналогия, обусловленная изоморфным замещением элементов, распространена значительно шире. Так как возможность изоморфного замещения обусловлена преимущественно размерным фактором, особенно при замещении катионообразователей, то этот вид диагональной аналогии обусловлен лишь малым различием атомных радиусов. Так, можно отметить близость орбитальных радиусов в диагональной паре Na-Са, что проявляется в широком изоморфизме этих элементов в силикатных и сложных оксидных системах. В то же время о глубокой химической аналогии между ними говорить нельзя, так как их силовые характеристики сильно различаются. Такие диагональные пары, аналогия между которыми проявляется в изоморфизме, достаточно многочисленны: Sc-Zr, Ti-Nb, V-Mo, Cu-Cd, Ag-Hg. Существует, однако, и обратная, или восходящая, диагональная аналогия такого типа ( от более тяжелого к более легкому элементу), наблюдающаяся у некоторых р-элементов-анионообра-зователей. Наиболее известны такие изоморфные пары: As-S, Sb-Se, Bi-Те, что проявляется во многих природных минералах. Так, наряду с диарсенидом железа FeAS, ( леллингит) и дисульфидом железа FeS2 ( пирит) широко распространен минерал арсенопирит FeAsS, который можно рассматривать как продукт изоморфного за-мещения серы или мышьяка в любом из предыдущих соединений. Аналогичные минералы известны, например, для кобальта и никеля. [23]
В случаях ( а) и ( в) разница в характерах связен А-S и В-S в конкретном соединении невелика, в то время как при комбинации ( б) атомы В и S образуют ковалентные комплексы, которые могут быть конечными или бесконечными в одном, двух или трех измерениях. Представителей класса ( в) среди оксосоединенип не найдено; более того, критерий для изоморфного замещения у сульфидов отличен от применяемого для сложных оксидов из-за более ионного характера связей в последних. В ионных соединениях возможность изоморфного замещения зависит главным образом от величины ионного радиуса, а химические свойства конкретного иона играют меньшую роль. Na гораздо чаще замещает приблизительно равновеликий с ним Са2, чем К, к которому он гораздо ближе по химическим свойствам. С другой стороны, в сульфидах критерием изоморфизма является способность разнородных атомов образовывать одинаковое число направленных связей; и действительно, атомы Си, Fe, Mo, Sn, Ag и Hg замещают Zn в сфалеритной и родственных ей структурах. [24]
Страницы: 1 2