Более сильная адсорбция
Cтраница 2
Способность элюента к специфическому взаимодействию с адсорбентом приводит к уменьшению селективности разделения ароматических углеводородов. При использовании в качестве элюента хлороформа и пропанола различие в удерживаемых объемах ароматических углеводородов, благодаря более сильной адсорбции элюента, уменьшается или даже совсем исчезает, поэтому эти элюенты непригодны для разделения ароматических углеводородов на исследованных адсорбентах. При разделении же специфически адсорбирующихся соединений, например ароматических аминов, применение специфически адсорбирующихся элюентов оказывается полезным. Так, о -, м - и и-нитроанилины при адсорбции из гексана удерживаются поверхностью, модифицированной амино-группами или мелоном, настолько сильно, что они вообще не детектируются у выхода из соответствующих колонн. При использовании же в качестве элюента хлороформа наблюдается различие в удерживании этих изомеров. [16]
Сопоставление найденных на висмуте адсорбционных пара метров с соответствующими величинами для ртутного электрода [76] показывает, что ориентация органических молекул в адсорбционном слое при 6 1 является на висмуте более вертикальной, чем на ртути. Вторым существенным различием адсорбционного поведения алифатических соединений на этих двух металлах является более слабая адсорбция высших членов гомологического ряда и более сильная адсорбция его низших членов на висмуте. Этот эффект проявляется особенно ясно при адсорбции спиртов и жирных кислот. Эти закономерности обусловлены значительным усилением специфического взаимодействия функциональной группы ( ОН, СООН) с поверхностью висмута по мере сокращения длины углеводородной цепи. [17]
Де Бур и Хоубен [6] объясняли аномально большой сдвиг спектров этих фенолов в красную область с помощью диаграммы на рис. 1 ( см. раздел II, Д), предположив, что энергия адсорбции для основного и возбужденного состояний сильно отличается. Они предположили, что большой батохромный сдвиг, наблюдаемый в подобных адсорбционных системах ( см. ниже), вызывается исключительно благодаря более сильной адсорбции возбужденной молекулы, в результате чего возбужденный уровень молекулы снижается в значительно большей степени, нежели ее основной уровень при адсорбции. [18]
В работе по выяснению влияния кристаллической структуры полученных испарением пленок металлов на скорость гидрирования [1] были установлены незначительные различия в адсорбции водорода пленками никеля, отложенными при комнатной температуре и при температуре жидкого воздуха. Это наблюдение противоречило всем другим имевшимся в литературе работам по адсорбции водорода на никелевых катализаторах, приготовленных восстановлением закиси никеля водородом, на которых была обнаружена более сильная адсорбция при высоких температурах. Кроме того, Бик с сотрудниками нашел в противоположность предшествовавшим исследованиям с восстановленными из закиси катализаторами, что адсорбция водорода на никелевой пленке происходит практически мгновенно как при комнатной температуре, так и при температуре жидкого воздуха; в литературе же сообщалось о медленной активированной адсорбции на типичных катализаторах гидрирования при повышенных температурах. Авторы получили изобары адсорбции водорода при давлении 0 1 мм рт. ст. в интервале температур от - 196 до 400; в результате этой работы было установлено, что форма изобары зависит от температуры, при которой пленка предварительно спекалась. [19]
При использовании слабоспецифического адсорбента - частично дегидроксилированного силохрома - замена элюента гексана на изо-пропанол приводит к обращению выхода из колонны ароматических углеводородов и их производных, содержащих способные к специфической адсорбции функциональные группы. Так, для нафталина, нитробензола и бромнафталина значения а при элюировании гексаном равны соответственно 1 3; 7 35 и 39 5, а при элюировании изопропа-нолом эти значения меньше и составляют соответственно 1 0, 0 6 и 0 23, что связано с более сильной адсорбцией изопропанола. [20]
Двойные связи, этерифициро-ванные гидроксильные группы, карбонильные и гидроксильные группы располагаются в приведенный ряд по усилению адсорбции. Сила адсорбции растет с увеличением числа каждой из этих групп. Сопряженные двойные связи вызывают более сильную адсорбцию, чем разобщенные двойные связи. Карбонильная группа, сопряженная с двойной связью, вызывает более сильную адсорбцию, чем каждая из этих групп в отдельности. [21]
Ионы фтора, калия или натрия совсем не адсорбируются на ртути. Если тенденция к адсорбции анионов электролита ( как, например, в растворах хлоридов, бромидов или иоди-дов щелочных металлов), выше, чем катионов, то потен-циал нулевого заряда более отрицательный, чем в таких растворах, как Кр или NaF. В то же время при более сильной адсорбции катионов по сравнению с анионами ( например, в растворе хлорида тетрабутиламмония) потенциал нулевого заряда более положителен. [22]
Обнаружено [90] 1, что стирол может тюлимеризоватьея с высокой скоростью при концентрациях эмульгатора ниже ККМ, если эмульгатор характеризуется хорошей адсорбционной способностью к поверхности стирола. Кроме того, установлено, что в процессе эмульсионной полимеризации стирола при равном и даже меньшем числе мицелл децилсульфата атрия по сравнению с числом мицелл додецилсульфата натрия в первом случае образуется больше частиц, что приводит соответственно к большей скорости полимеризации. Одним из возможных объяснений этого эффекта является более сильная адсорбция децилсульфата натрия поверхностью частиц полистирольного латекса. [23]
В реакциях алкилирования модифицированные фожазиты, HY 24 ], а также CaY [16] используют более широко, чем СаХ, NaX и НМ. В работе [24] проведено алкилирование различных углеводородов олефинами, спиртами, эфирами и др. На фожазитах, HY и ( P33) Y реакции в жидкой фазе идут более эффективно, так как уменьшается скорость старения катализаторов, связанная с окклюзией больших молекул полиядерных углеводородов, неспособных выйти из полостей цеолита. Присутствие в цеолите гидроксильных групп приводит к более сильной адсорбции фенола; при этом температура, необходимая для этилирования фенола, должна быть выше, чем при эти - чировании бензола. [24]
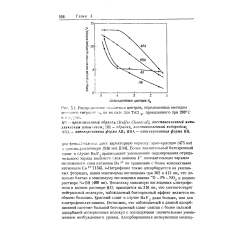 |
Распределение кислотных центров, определенных методом ацл. т.й. ого титрсяжн - я, по их силе для TiCl 3, прокаленного при 200 С в Е - - уме. [25] |
Поскольку максимум поглощения - нитрофенола в водном растворе НС1 приходится на 316 нм, что соответствует нейтральной молекуле, наблюдаемый батохромныи эффект является необычно большим. Возможно, что наблюдаемый в данной адсорбционной системе большой батохромныи сдвиг связан с более сильной адсорбцией возмущенных молекул с последующим значительным уменьшением возбужденного уровня. [26]
Подобные результаты были получены Киплингом [121] при изучении адсорбции бинарных жидких смесей углеводородов. Графой имеет намного более однородную поверхность и почти свободен от кислородсодержащих комплексов. Более сильную адсорбцию уксусной кислоты и метилацетата на сфероне-6, чем на графоне, Райт объясняет большей полярностью поверхности сферона-6 из-за присутствия на поверхности сферона-6 кислородных комплексов. Менее полярная стеариновая кислота с большей, чем у уксусной кислоты, длиной цепи адсорбируется лучше на графоне, чем сфероне-6. В последнее время появились работы, относящиеся к изучению влияния химии поверхности активного угдя на адсорбцию органических веществ - неэлектролитов и слабых электролитов - из водных растворов. [27]
Двойные связи, этерифициро-ванные гидроксильные группы, карбонильные и гидроксильные группы располагаются в приведенный ряд по усилению адсорбции. Сила адсорбции растет с увеличением числа каждой из этих групп. Сопряженные двойные связи вызывают более сильную адсорбцию, чем разобщенные двойные связи. Карбонильная группа, сопряженная с двойной связью, вызывает более сильную адсорбцию, чем каждая из этих групп в отдельности. [28]
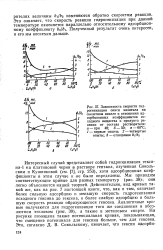
Интересный случай представляет собой гидрогенизация гекси-на-1 на платиновой черни о растворе гептана, изученная Сокольским и Кушниковой ( см. [7], стр. В этом случае и не были определены. Мы приводим соответствующие кривые для разных температур ( рис. 38); они легко объясняются нашей теорией. Действительно, вид кривых такой же, как на рис. 7 настоящей книги, что, как и там, означает более сильную адсорбцию и меньшую скорость гидрогенизации исходного гексина до гексена, и более слабую адсорбцию и большую скорость реакции образующегося гексена. Аналогичные кривые получаются для гидрогенизации того же соединения в абсолютном этиловом ( рис. 39), а также в метиловом спирте. На рисунке помещена также потенциальная кривая, показывающая, что смещение потенциала для гексина больше, чем для гексена. [30]
Страницы: 1 2 3