Сильная специфическая адсорбция
Cтраница 2
Особое влияние оказывают на полярографические волны катионы тетраалкиламмония, которые способны к сильной специфической адсорбции. Поэтому введение в состав фона этих ионов в значительной мере усиливает каталитический ток. [16]
Анализ этого уравнения, а также сравнение с экспериментом ( Парсонс [44]) показывают, что в случае сильной специфической адсорбции величина коэффициента Есина и Маркова не зависит от плотности заряда. [17]
Монослой молекул обычных размеров будет прочно удерживаться на поверхности при температурах колонки только в случае, если его молекулы будут связаны с поверхностью химически ( за счет проведения соответствующих поверхностных реакций) или же при очень сильной специфической адсорбции. Поэтому в качестве наносимых веществ использовались пары специфически адсорбирующихся на силикагеле полярных соединений. Предполагая, что при температуре на 10 - 20 С выше температуры кипения наносимого вещества образуется преимущественно монослой, в колонку, наполненную адсорбентом-носителем, с потоком газа-носителя при соответствующей температуре вводились пары моноэтаноламина, триэтаноламина, триэтиленгликоля и бути-рата триэтиленгликоля до насыщения адсорбента. С этой целью в колонку последовательно дозировалось по 10 мкл соответствующей жидкости. [18]
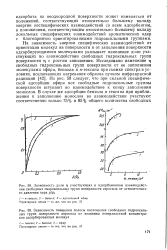 |
Зависимость смещения полосы поглощения свободных гидроксильных групп поверхности аэросила от величины поверхностной концентрации адсорбированных молекул. [19] |
На зависимость энергии специфических взаимодействий от ориентации молекул на поверхности и от заполнения поверхности адсорбирующимися молекулами указывает изменение доли участвующих во взаимодействии свободных гидроксильных групп поверхности ц с ростом заполнения. Из рис. 58 следует, что при сильной специфической адсорбции эфира все свободные гидроксильные группы поверхности вступают во взаимодействие к концу заполнения монослоя. [20]
В работе [33] отмечено, что рост интенсивности полосы поглощения гидроксильных групп, связанных с атомом бора ( с частотой 3703 СМ 1), указывает на миграцию атомов бора из объема пористого стекла на его поверхность. Эти авторы считают, что такие примесные атомы являются центрами сильной специфической адсорбции, которая приписывалась в ряде рассмотренных выше работ центрам второго рода. К настоящему времени получено много спектральных доказательств прочной специфической адсорбции на примесных центрах пористого стекла. [21]
В разделе 1а отмечалось, что аномальный сдвиг потенциала нулевого заряда при изменении концентрации аниона для сильной специфической адсорбции был приписан влиянию дискретности заряда. Автором этой идеи Есин и Марков [2] считают Фрумкина [37], и к этому можно добавить, как отметил Парсонс [34], что де Бур [38] независимо развил подобные представления для адсорбции на границе металл - газ. [22]
Неспецифические адсорбенты с особенно однородной поверхностью удобно применять также для выделения воды раньше других компонентов. Что касается таких адсорбентов, как обычные силикагели, то их можно применять для разделения неспецифически и слабо специфически адсорбирующихся молекул. По мере увеличения размеров молекулы необходимо уменьшение удельной поверхности и расширение пор адсорбента, а для веществ, способных к сильной специфической адсорбции, следует применять неспецифические адсорбенты с возможно более однородной поверхностью, а также следует увеличивать температуру колонки. [23]
Отравление катализаторов металлами или производными металлов в случае никелевых контактов исследовано в меньшей степени, чем в случае платиновых. Одна из ранних работ в этой области принадлежит Уэно [27], который изучал токсичность мыл, образуемых рядом металлов, по отношению к никелевому катализатору гидрирования. Он нашел, что мыла тяжелых металлов - цинка, кадмия, свинца, ртути, висмута и олова - токсичны; однако такие вещества, как мыла, обычно находящиеся в коллоидном состоянии или s виде несовершенных растворов, могут, весьма вероятно, отравлять контакт не только вследствие сильной специфической адсорбции, но и вследствие обволакивания поверхности, так что список токсичных и нетоксичных мыл, составленный Уэно, возможно, следует пересмотреть с этой точки зрения. Это в особенности касается мыл щелочных металлов, магния и бария, которые, как установлено, могут снижать активность катализаторов. [24]
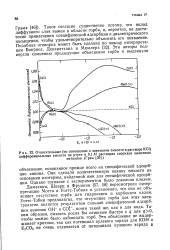 |
Относительные ( по отношению к значениям емкости в растворе КС1 дифференциальные емкости на ртути в 0 1 М растворах хлоридов щелочных. [25] |
Однако согласие с экспериментом было довольно плохим. Дамаскин, Шварц и Фрумкин [57, 58] пересмотрели интерпретацию Мотта и Уоттс-Тобина и установили, что она не объясняет отсутствие горба для гидроокиси и карбоната калия. Уоттс-Тобин предполагал, что отсутствие горба для этих электролитов является результатом сильной специфической адсорбции анионов ОН - и СОз - почти такой же, как и для иода. Таким образом, емкость росла бы слишком быстро с q для q0, чтобы можно было наблюдать горб. [26]
В [1 ] было показано, что в гликолевых растворах действительно наблюдается резкое увеличение адсорбируемости катионов. По результатам настоящей работы видно, что поверхностная активность анионов в гликолевых растворах, по сравнению с водными, резко уменьшается. Из сопоставления данных настоящей работы с данными работ, проведенных для других неводных растворителей, видно, что величина поверхностной активности анионов мало зависит от величины макроскопической диэлектрической постоянной растворителя ( D) и в основном определяется энергией их сольватации. Из растворов диметилформамида, ди-метилсульфоксида и сульфолана, наоборот, наблюдается сильная специфическая адсорбция анионов [3, 9], так как в этих апротонных растворителях они слабо сольватированы. D независимо от типа растворителя. Например, в гликолевых ( D37 7) и диметилформамидных ( D36 7) [3] растворах ряд адсорбционной активности анионов почти совпадает, несмотря на то, что гликоль является протонным, а диметилфор-мамид - апротонным растворителем. [27]
Грэм [29] предположил существование некоторой ковалент-ной связи между специфически адсорбированными анионами и ртутью. В качестве доказательства, подтверждающего это предположение, он привел линейную зависимость между дифференциальной емкостью при предельно положительных потенциалах, при которых только могут быть проведены измерения, и логарифмом концентрации ионов ртути в солях, соответствующих данному аниону. Эта интерпретация природы специфической адсорбции была отвергнута Левиным, Беллом и Кальвертом [31], которые считали причиной специфической адсорбции - действие сил изображения ( см. раздел 4 этой главы), и Бокрисом, Дева-натханом и Мюллером [32], которые утверждали, что степень и тип ионной гидратации являются главным фактором, который необходимо учитывать. Эти данные относятся к условиям, очень отличным от тех, которые существуют на поверхности раздела ртуть / раствор, но эта оговорка вряд ли может быть причиной такого расхождения. Бокрис и др. полагают, что ионы с высоким первичным числом гидратации обнаруживают малую склонность к специфической адсорбции, тогда как ионы с низким числом первичной гидратации проявляют сильную специфическую адсорбцию, в случае если электростатическое отталкивание не слишком велико. [28]
Страницы: 1 2