Участник - реакция
Cтраница 3
А - - участники реакции; v; - числа молей. [31]
А, - участники реакции; v - - числа молей. [32]
 |
Уровни энергии мо. [33] |
А - - участники реакции; v - - числа молей. [34]
Реагентом считается тот участник реакции, который обладает большей энергией. Чаще всего это свободные радикалы или ионы, которые образуются в результате разрыва связей. [35]
Конденсированные реагенты - участники заданной реакции при изменении температуры претерпевают аллотропические и агрегатные превращения, которые должны быть учтены даже при проведении приближенных расчетов. [36]
В этом случае полифункциональные участники реакции присоединяются друг к другу без отщепления части молекул, как это происходит в случае поликонденсации. Ступенчатая полимеризация обнаруживает таким образом схематическое сходство с полимеризацией. Однако в этом случае, как и при поликонденсации, каждая отдельная ступень реакции независима от предыдущей. [37]
В расчет принимаются только газообразные участники реакции. [38]
Расчетные скорости образования участников реакции являются линейными комбинациями скоростей стадий и в выражение для скорости стадии всегда в качестве множителя входит кинетическая константа. [39]
Изучение процессов хемосорбции участников реакции в предкаталитической и каталитической областях температур является одним из путей изучения свойств поверхности окисных катализаторов и соответственно причин изменения избирательности их действия. [40]
Если известны активности участников реакций в растворе, константы ki и k %, коэффициенты oci и рг, то вычисление фс возможно. Применимость уравнения ( V15) определяется тем, насколько подробно и достоверно исследована кинетика каждой из сопряженных реакций. [41]
Меняя количественное соотношение участников реакции и другие условия ее проведения, можно получить продукт взаимодействия ацетилена как с одной, так и с двумя молекулами карбонильного соединения. Аналогичным образом реагирует и винил-ацетилен. [42]
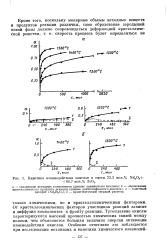 |
Кинетика взаимодействия окислов в смеси мол. % Nd203. [43] |
От кристаллохимических факторов участников реакций зависит и диффузия компонентов к фронту реакции. Тугоплавкие окислы характеризуются высокой прочностью химических связей между ионами, чем объясняется большая величина энергии активации взаимодействия окислов. [44]
Теплоемкость каждого из участников реакции тоже зависит от температуры. Зависит от температуры поэтому и ДСР, Но установить зависимость СР ( равным образом и Су) от температуры методами термодинамики уже нельзя. Желая вывести термодинамическое уравнение для производной дСР / дТ, мы прибегаем к теореме о независимости смешанных частных производных от последовательности дифференцирования. Но тогда мы увидим ( если не увидели раньше), что само СР является производной от ряда термодинамических величин ( например, Я, S) по температуре. Следовательно, поставленная задача не решается методами термодинамики. [45]
Страницы: 1 2 3 4