Изучение - равновесие
Cтраница 1
Изучение равновесия жидкость - пар является одним из наиболее сложных элементов проблемы исследования ректификации промышленных смесей. С увеличением числа компонентов трудности исследования возрастают из-за сложности определения составов фаз и необходимости проведения большого числа экспериментов для получения данных в достаточно широком диапазоне концентраций. Работа в этом направлении привела к выводу ряда уравнений [1-5], позволяющих рассчитывать фазовые равновесия в многокомпонентных смесях на основе бинарных равновесных данных, полученных экспериментально. [1]
Изучение равновесия и движений тела человека было предпринято Н. А. Бернштейном, создавшим точную и совершенную методику изучения этих движений и давшим методы математического анализа их. [2]
Изучение равновесия и устойчивости различных гравитирующих систем должно, по-видимому, сыграть важную роль в построении картины их эволюции. Моменты, когда система теряет устойчивость, определяют критические точки линии эволюционного развития, когда плавная эволюция системы должна смениться быстрой перестройкой. Некоторые авторы [195] действительно отмечают следы скачкообразных изменений, имевших место в нашей Галактике. С другой стороны, плавная эволюция должна, очевидно, идти вдоль последовательности квазистационарных состояний. Это аналогично ситуации в мире звезд [150], где диаграмма спектр - светимость показывает наличие в заметном количестве только звезд в известных своей квазистационарностью участках диаграммы ( прежде всего на главной последовательности): участки, соответствующие сильно нестационарным состояниям, быстро проскакиваются эволюционирующей системой. [3]
Изучение равновесий и кинетики реакций преобразования состава Г11В сильно осложняется поликомпонентным составом как твердой, так и жидкой фаз, их взаимовлиянием. Кроме того, как состав отдельных минералов, так и их соотношение друг с другом в объеме породы значительно варьируют даже в пределах одной литологи-ческой пачки; значительно меняется также содержание органического вещества. Все это осложняет применение данных по отдельным экспериментально изученным реакциям к конкретным природным объектам. [4]
Изучение равновесия в насыщенных растворах сильных электролитов ( например, солей) дает возможность выяснить условия, вызывающие образование или растворение осадков в этих растворах. При растворении кристаллов электролитов с ионной кристаллической решеткой в раствор переходят не молекулы, а ионы. [5]
Изучение равновесий в системах: соли металлов - окислы металлов - вода. [6]
Изучение равновесий двух несмешивающихся жидкостей во фторосиликатных системах, содержащих щелочные металлы, являющихся аналогами подобных же водносиликатных систем, имеет значение для исследования ликвационных явлений в природных магмах. [7]
Изучение равновесия в насыщенных растворах сильных электролитов ( например солей) дает возможность выяснить условия, вызывающие образование или растворение осадков в этих растворах. При растворении кристаллов электролитов, построенных из ионов, в раствор переходят не молекулы, а ионы. [8]
Изучение равновесия жидкость - пар показывает, что смесь NbCl 5 - ТаС1 5 образует почти идеальный раствор, следующий закону Рауля, Подсчитано, что для разделения NbCl5 и ТаС15 на продукты 99 9 % - ной чистоты необходима колонна с 48 теоретическими тарелками. [9]
Изучение равновесия жидкость - пар является одним из наиболее сложных элементов проблемы исследования ректификации промышленных смесей. С увеличением числа компонентов трудности исследования возрастают из-за сложности определения составов фаз и необходимости проведения большого числа экспериментов для получения данных в достаточно широком диапазоне концентраций. Работа в этом направлении привела к выводу ряда уравнений [1-5], позволяющих рассчитывать фазовые равновесия в многокомпонентных смесях на основе бинарных равновесных данных, полученных экспериментально. [10]
Изучение равновесия в насыщенных растворах сильных электролитов ( например, солей) дает возможность выяснить условия, вызывающие образование или растворение осадков в этих растворах. При растворении кристаллов электролитов, с ионной кристаллической решеткой, в раствор переходят не молекулы, а ионы. [11]
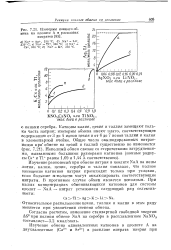 |
Изотермы ионного обмена на цеолите А в расплавах нитратов. [12] |
Изучение равновесий при обмене натрия в цеолите NaA на ионы лития, калия, цезия, серебра и таллия показало, что полное замещение катионов натрия происходит только при условии, если большие а-полости могут окклюдировать соответствующие нитраты. В противном случае обмен является неполным. [13]
Изучение равновесия показало, что устойчивость карбанионов уменьшается в ряду винил фенил циклопропил этил пропил изобутил неопентил циклобутил циклопентил. [14]
Изучение равновесия в насыщенных растворах сильных электролитов ( например, солей) дает возможность выяснить условия, вызывающие образование или растворение осадков в этих растворах. При растворении кристаллов электролитов с ионной кристаллической решеткой в раствор переходят не молекулы, а ионы. [15]
Страницы: 1 2 3 4