Изучение - фазовое равновесие
Cтраница 4
При изучении фазовых равновесий в среде сжиженных газов и при количественных анализах ИК-спектроскопия обнаруживает ряд преимуществ по сравнению с другими методами физико-химических исследований. Во-первых, спектроскопия дает возможность непосредственно в растворе обнаруживать присутствие как растворенного вещества, так и его кристаллической фазы, поскольку спектры веществ в различных фазовых состояниях, как правило, сильно отличаются друг от друга. В-третьих, высокая чувствительность метода, которая практически ограничивается только прозрачностью растворителя, позволяет обнаруживать весьма малые концентрации растворенного вещества ( порядка 10 - 8 мол. Все эти соображения свидетельствуют о перспективности применения ИК-спектроскопии в физико-химических исследованиях низкотемпературных систем и в задачах, представляющих интерес для промышленной криогеники. В настоящей статье обобщаются результаты исследований спектров растворов различных соединений, многие из которых встречаются в виде примесей к техническим сжиженным газам - кислороду, аргону, азоту. [46]
При изучении фазовых равновесий в системах окислов, содержащих элементы с переменной степенью окисления, необходим очень тщательный контроль состава и давления газовой фазы, так как при установлении равновесия решающее влияние оказывает парциальное давление кислорода в газовой фазе. [47]
При изучении фазовых равновесий в системе Ni-V было найдено, что в сплаве № 25 % ( ат. [48]
При изучении фазовых равновесий широко используется графический метод. Соответствующие диаграммы называются фазовыми диаграммами, или диаграммами состояния. Они строятся на основе опытных данных. [49]
При изучении фазового равновесия в системе жидкость - пар бинарной смеси SiHCl3 - СН3СООС2Н5 возникла необходимость количественного анализа данной смеси на содержание одного из составляющих ее компонентов. Достаточно надежных химических методов анализа для смесей, подобных данной, в литературе не описано. Поэтому предпринята попытка разработать спектрофотометрический метод анализа по спектрам поглощения в ИК-области. Принципиально оказалось возможным вести анализ по максимуму полосы поглощения этилацетата v 1760 см 1, так как трихлорсилан не имеет полос поглощения в этой области. [50]
 |
Фазовое равновесие жидкость - пар в системе синильная кислота - цианистый аллил. [51] |
При изучении фазовых равновесий жидкость - пар в системах синильная кислота - акролеин и синильная кислота - акролеин - акрилонитрил при 400 мм рт. ст. было установлено60, что в бинарной системе синильная кислота - акролеин коэффициент разделения а увеличивается с возрастанием содержания синильной кислоты в жидкой фазе. В тройной системе с акрилонитрилом коэффициент разделения а между синильной кислотой и акрилонитрилом остается практически таким же, как и в бинарной системе, в то время как коэффициент разделения а. [52]
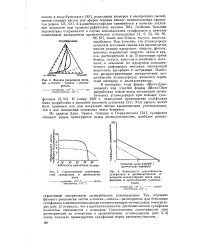
Так, изучение фазового равновесия систем к-гептан-ксилол-растворитель для безводных сульфолана и диэтиленгликоля при соответствующих оптимальных температурах ( рис. 2) показало, что в противоположность диэтиленгликолю сульфолан полностью смешивается с ксилолом. [54]
Экспериментальные трудности изучения фазовых равновесий в многокомпонентных системах, как известно, чрезвычайно велики. В связи с этим, как нам кажется, актуальное значение имеют работы Кравченко [23, 44], которые являются первыми попытками теоретического обобщения экспериментальных данных о физико-химическом анализе двойных систем парафиновых углеводородов с целью выяснения закономерностей взаимодействия их компонентов, изыскания методов расчета простейших типов четверных и пятерных систем. [55]
Надежность результатов изучения фазовых равновесий и фазовых превращений органических веществ в значительной мере зависит от истинной чистоты и действительной индивидуальности изучаемых соединений. Это обусловлено влиянием разнообразных загрязнений, даже весьма малого процента, на характер фазовых превращений. [56]
Предложен метод изучения фазового равновесия жидкость - пар для систем, содержащих один из компонентов в мпкроконцентрации, без отбора проб. [57]
Опыты по изучению фазовых равновесий в системе диметил-нафталин - тиомочевина - растворитель проводились следующим образом. К тиомочевине, пропитанной активатором ( метанол), при постоянном перемешивании прибавляли сырье - раствор 2 3-диметилнафталина в н-тридекане. [58]
Если при изучении фазовых равновесий окажется, что в системе образуются твердые комплексные соединения, то в расплаве комплексообразование возможно. Этот вывод вполне обоснован, поскольку структуру расплава можно рассматривать как неупорядоченную структуру твердого тела, и в расплаве, вероятно, существуют ионы, подобные тем, которые имеются в твердом веществе. [59]
Страницы: 1 2 3 4