Изучение - термический распад
Cтраница 1
Изучение термического распада полистирола, проведенное Земани [2209] позволило получить величину энергии активации образования бензола, толуола и стирола из полимера. [1]
Изучение термического распада ГПИПБ позволяет также выявить воздействие растворителя на гидронероксид. [3]
Изучению термического распада пространственных полимеров посвящено большое число работ, однако установить научно обоснованные критерии пригодности полимеров для получения УВМ труднее, чем для линейных полимеров. [4]
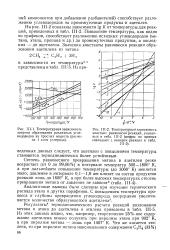
При изучении термического распада сополимера трифторхлор-этилена со фтористым винилиденом было установлено [34], что при температурах 200 - 300 С в вакууме отщепляется НС1 и HF. Энергия активации отщепления галоидоводородов от эластомера типа Kel-F в указанном интервале температур равна для НС1 29 ккал и для HF 34 ккал. [5]
 |
Термическая стабильность смазочных материалов, оцененная масс-спектрометрическим методом. [6] |
Достоинством масс-спектрометрического метода изучения термического распада смазочных материалов является возможность изучения причин нарушения их термической стабильности. [7]
Аналогичные выводы были сделаны при изучении термического распада этана и других парафинов. [9]
Проведенные опыты подсказали, с другой стороны, оригинальный метод для изучения термического распада при тех температурах, при которых скорость реакции столь велика, что ее нельзя измерять классическими методами, пригодными для температур 500 С. Из теории цепных реакций известно, что длина реакционной цепи должна уменьшаться с повышением температуры; иначе говоря, при 800 - 900 С число актов зарождения и обрыва цепи увеличивается по сравнению с температурами, при которых обычно измеряется скорость реакции. [10]
Проведенные опыты подсказали, с другой стороны, оригинальный метод для изучения термического распада при тех температурах, при которых скорость реакции столь велика, что ее нельзя измерять классическими методами, пригодными для температур си 500 С. Из теории цепных реакций известно, что длина реакционной цепи должна уменьшаться с повышением температуры; иначе говоря, при 800 - 900 С число актов зарождения и обрыва цепи увеличивается по сравнению с температурами, при которых обычно измеряется скорость реакции. [11]
Разложение в начальной стадии кетена с образованием метиленового радикала было еще ранее доказано при изучении термического распада кетена. [12]
С точки зрения взаимного влияния атомов в органическом соединении любопытно обратить внимание на существенное отличие в распаде 1 2 - и 1 1-дихлорэтана. При изучении термического распада последнего оказалось, что в противоположность 1 2-дихлор-этану добавка кислорода, а также пропилена и уксусного альдегида не оказывает влияния на скорость распада 1 1-дихлорэтана. [13]
Изучение процесса термической диссоциации на примере таких простых по химическому строению и составу соединений, какими являются алканы, важно для выяснения величин энергий индивидуальных химических связей органических соединений, а также решения тонкого вопроса о взаимном влиянии связей в молекуле с различной длиной и строением углеродной цепи. Весьма заманчиво использовать изучение термического распада регулярно построенных алканов в целях химической кинетики - выяснения влияния длины углеродной цепи и ее строения на динамические параметры реакций распада ( энергия активации, стерический фактор и др.) и построения моделей или механизма превращений. Дрстаточно напомнить, что учение о мономолекулярных реакциях и теория этих процессов - большой раздел химической кинетики, который в значительной степени опирается на экспериментальное изучение реакций термической диссоциации различных соединений, в том числе и углеводородов. [14]
Из сопоставления этого числа с приведенными выше теоретическими значениями величины k: k для двух механизмов распада следует, что истинный механизм реакции отвечает молекулярной схеме С2Н5Вг С2Н4 НВг. Заметим, что этот результат получается также и из данных по изучению термического распада бромистого этила при помощи так называемого толуольного метода ( см. ниже, стр. [15]
Страницы: 1 2