Изучение - реакция
Cтраница 2
Изучение реакций, которым подвергаются тела, ведет, далее, к понятию о химической частице и выражению веса и состава частиц частичными формулами. [16]
Изучение реакций, протекающих как в присутствии, так и в отсутствие катализаторов, раскрыло важную сторону механизма их действия, которое заключается в том, что катализаторы уменьшают энергию активации реакций. Например, известно, что энергия активации гомогенной реакции в газовой фазе - разложения йодистого водорода 2HI - Н2 12 - равна 44 3 ккал / моль ( стр. Энергия активации этой реакции, проводимой в присутствии металлического золота в качестве катализатора ( гетерогенный катализ), равна 25 ккал / моль, а в присутствии платины - только 14 ккал / моль. Энергия активации некаталитического разложения перекиси водорода в водном растворе равна 18 ккал / моль. [17]
Изучение реакции триэтилгидроксисилана со спиртами [218] показало, что и в этом случае происходит образование триэтилалкоксиси-ланов. [18]
Изучение реакции диэтилдиэтоксисилана с формальдегидом ( парафор-мом) показало, что увеличение продолжительности нагревания приводит к получению смеси полидиэтилсилоксанов с повышенным содержанием этоксильных групп. [19]
Изучение реакции продолжается на ряде аналогичных гликолей. [20]
Изучение реакций, происходящих в высокотемпературной дейтериевой плазме ( 111.3.6.1), является теоретической основой получения искусственных управляемых термоядерных реакций. Основной трудностью является поддержание условий, необходимых для осуществления самоподдерживающей-с я термоядерной реакции. Для такой реакции необходимо, чтобы скорость выделения энергии в системе, где происходит реакция, была не меньше, чем скорость отвода энергии от системы. При температурах порядка 108 К термоядерные реакции в дейтериевой плазме обладают заметной интенсивностью и сопровождаются выделением большой энергии. [21]
Изучение реакций, происходящих в высокотемпературной дейтериевой плазме ( 111.3.6.1), является теоретической основой получения искусственных управляемых термоядерных реакций. Основной трудностью является поддержание условий, необходимых для осуществления самоподдерживающейся термоядерной реакции. Для такой реакции необходимо, чтобы скорость выделения энергии в системе, где происходит реакция, была не меньше, чем скорость отвода энергии от системы. При температурах порядка 108 К термоядерные реакции в дейтериевой плазме обладают заметной интенсивностью и сопровождаются выделением большой энергии. [22]
Изучение реакции VC14 с КхА12С1б - х для х 2 - 6 показало, что скорость алкилирования ( и восстановления) ванадия понижается с уменьшением количества алкиль-ных групп в АОС. [23]
Изучение реакций очень часто ведут в лабораторных аппаратах периодического действия с дальнейшим использованием полученных результатов в установках непрерывного действия. [24]
Изучение реакций, происходящих в процессе каталитического крекинга нефтепродуктов, а также лри различных способах облагораживания бензинов, привело к выводу о том, что дегидрогенизация шестичленных циклов происходит и под влиянием алю-мосиликатных катализаторов. При 540 С некоторые алкилцикло-гексаны, по их наблюдениям, на 20 % превращались в ароматические углеводороды. [25]
Изучение реакции при более высокой температуре, порядка 145 - 165, показало, что уксусная кислота в этих условиях, алкилируется бутеном-2 очень быстро, и максимальный выход втор. [26]
Изучение реакций с участием макромолекул составляет большой раздел химической кинетики. При описании подобных реакций обычно применяют теорию случайных процессов. Чтобы упростить задачу описания реакции типа замещения, макромолекулы рассматривают как бесконечно длинные цепочки, исключая таким образом влияние концов. В этом параграфе используется вероятностный подход к описанию кинетики реакций с участием макромолекул и дается применение теории марковских процессов к таким задачам. [27]
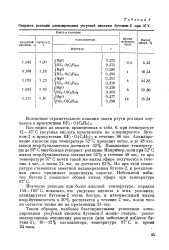 |
Скорость реакции алкнлвровавия уксусной кислоты бутеном-2 при 97 С. [28] |
Изучение реакции при более высокой температуре, порядка 145 - 165 С, показало, что уксусная кислота в этих условиях, алкилируется бутеном-2 очень быстро, и максимальный выход втор. [29]
Изучение реакций между твердыми веществами в тех случаях когда ни одно из участвующих веществ не является летучим соединением, представляет некоторые трудности, чем и объясняется главным образом медленность прогресса в этой области. Для понимания механизма такой реакции необходимо идентифицировать все ее промежуточные и конечные продукты, измерить скорость всех бинарных взаимодействий между компонентами и составить ясное представление о структурном характере системы во всех стадиях процесса. [30]
Страницы: 1 2 3 4