Учет - отталкивание
Cтраница 1
Учет водородного отталкивания, конечно, привел бы к увеличению валентного угла, как и применение гибридных s - р-орбит для атома кислорода. [1]
Учет отталкивания электронов сводится к частичному экранированию ими ядра атома, что приводит к двум эффектам. Прежде всего все уровни энергии в сравнении с (10.27) поднимаются за счет замены Z на эффективный заряд ядра Z3 ()) Z. Электроны с большими значениями / находятся, как известно, в среднем дальше от ядра, так что экранирование их более эффективно. Поэтому соответствующие уровни поднимаются выше. В то же время электроны с малыми / могут находиться вблизи ядра, где экранирование мало, так что соответствующие уровни меняются незначительно. [2]
Необходимость учета отталкивания между электронами чрезвычайно усложняет расчет волновых функций и энергетических уровней электронов в многоэлектронных атомах. Поэтому в случае многоэлектронных систем используют различные приближения, среди которых наиболее широко применяется одноэлектронноеприближение. В его основе лежит представление о существовании индивидуальных состояний каждого электрона в некотором эффективном поле, создаваемом ядром и всеми остальными электронами. Эти состояния описываются соответствующими одноэлектронными волновыми функциями, из которых может быть сконструирована полная волновая функция многоэлектронной системы. [3]
Необходимость учета отталкивания между электронами чрезвычайно усложняет расчет волновых функций и энергетических уровней электронов в многоэлектронных атомах. Поэтому в случае многоэлектронных систем используют различные приближения, среди которых наиболее широко применяется одноэлектронное приближение. В его основе лежит представление о существовании индивидуальных состояний каждого электрона в некотором эффективном поле, создаваемом ядром и всеми остальными электронами. Эти состояния описываются соответствующими одноэлектронными волновыми функциями, из которых может быть сконструирована полная волновая функция многоэлектронной системы. [4]
В [31] была сделана попытка учета отталкивания исключением области малых расстояний между нуклонами. При этом теряется влияние отталкивания на эффективный потенциал, действующий на нуклон. По-видимому, в этом причина того, что в [31] получается заниженное значение для критической плотности. Благодаря я-конденсации монотонный рост эффективного поля нарушается, однако и в этом случае эффективный потенциал имеет порядок тп и недостаточен для того, чтобы скомпенсировать иуклопную массу. [5]
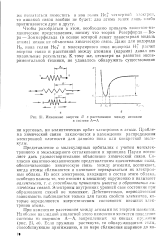 |
Изменение энергии U с расстоянием между атомами в системе А-А. [6] |
Представление о молекулярных орбиталях с учетом межэлектронного и межъядерного отталкивания и принципа Паули позволяет дать удовлетворительное объяснение химической связи. Согласно квантово-механическим представлениям значительные силы, обеспечивающие химическую связь между атомами, возникают, когда атомы сближаются и начинают перекрываться их электронные облака. Электроны внутренних уровней свое состояние при образовании связей не изменяют. Действительно, периодическая зависимость наблюдается только для таких свойств элементов, которые определяются энергетическим состоянием внешних электронов атома. [7]
Тогда первое приближение следует получать уже с учетом отталкивания между электронами каждого атома в отдельности, вводя таким образом динамическое различие между двумя типами электронов. Эта процедура, естественно, имеет смысл только до тех пор, пока расстояние d между атомами велико по сравнению с их линейными размерами а. То, что % и i) t / не могут вместе образовать ортогональную систему ( на самом деле они даже не являются линейно независимыми, поскольку уже одни г) / образуют полную ортогональную систему), приводит к некоторому затруднению. [8]
Из приведенного вывода ясно, что при учете отталкивания частиц в хемосорбционном слое уравнение логарифмической изотермы получается только в результате сделанных упрощений в уравнении состояния, а реальное положение дел более точно передается выражением (11.20), не содержащим логарифма. [9]
Следующий шаг в усовершенствовании электростатической модели связан с учетом отталкивания между обменными катионами. Для дегидратированного Са-фожазита, содержащего 28 ионов Са, минимальное отталкивание достигается при заполнении только мест I и II. [10]
 |
Зависимость теплоты адсорбции водорода на никеле от степени покрытия подложки водородом. [11] |
Теоретическое объяснение зависимости теплоты адсорбции от степени покрытия исходит из учета отталкивания между л-адатома-ми. Атомарный водород интенсивно адсорбируется также на поверхности элементарных полупроводников. Одной из возможных форм адсорбции является погружение малых по размерам атомов водорода под поверхность кристалла. Для молекулярного водорода характерно ничтожно малое ( примерно 10 - 4 монослол) покрытие поверхности даже при ЮО С. Многие сложные полярные молекулы, содержащие радикалы с концевым атомом водорода, также хорошо адсорбируются на германии. К таким веществам относятся вода, СН3ОН; ( СНз) гО, СН3СООН и др. Общая структурная особенность таких соединений состоит в наличии у них конфигураций, при которых атом водорода может находиться в непосредствен-иом контакте с поверхностью rep - мания. Предполагается, что другие сложные соединения типа N2, CO, СО2) СН4, СС14, СН3С1, ( С2Н5) 20, СбНе на поверхности Ge в заметных количествах не адсорбируются потому, что они либо не содержат атомов водорода, либо последние не образуют сильной полярной связи в молекуле. [12]
 |
Схема энергетических уровней атома кислорода. [13] |
Нетрудно понять, чем будут отличаться эти орбитальные заселенности при учете отталкивания между электронами. [14]
Конечно, метод МОХ основан на очень простой модели молекулы, и возможные уточнения техники расчета не исчерпываются учетом отталкивания электронов. Мы не можем рассматривать здесь эту проблему в общем плане, поскольку ее обсуждение не имеет близкого отношения к собственно карбо-ниевым ионам. [15]
Страницы: 1 2 3