Учет - отталкивание
Cтраница 3
Ацетилен обладает менее кислыми свойствами, чем вода, но он в 1013 раз более сильная кислота, чем аммиак, и по крайней мере в 1018 раз сильнее как кислота, чем этилен или этан. Большая кислотность ацетилена и алки-нов-1 по сравнению с другими углеводородами находит простое объяснение при учете отталкивания между электронной парой связи С - Ни другими электронами атома углерода ( см. стр. Сравним С - Н - связи в ацетилене и алкане. Прежде всего заметим, что шесть электронов тройной связи ацетилена заключены в пространстве между двумя ядрами атомов углерода. В результате эти электроны располагаются в среднем дальше от электронной пары С - Н - свЯзи, чем шесть электронов насыщенного тетраэдрического углерода. [31]
Ацетилен обладает менее кислыми свойствами, чем вода, но он в 1013 раз более сильная кислота, чем аммиак, и по крайней мере в 1018 раз сильнее как кислота, чем этилен или этан. Большая кислотность ацетилена и алки-нов-1 по сравнению с другими углеводородами находит простое объяснение при учете отталкивания между электронной парой связи С - Ни другими электронами атома углерода ( см. стр. Сравним С - Н - связи в ацетилене и алкане. Прежде всего заметим, что шесть электронов тройной связи ацетилена заключены в пространстве между двумя ядрами атомов углерода. В результате эти электроны располагаются в среднем дальше от электронной пары С - Н - связи, чем шесть электронов насыщенного тетраэдрического углерода. [32]
Точно таким же способом, как и выше, могут быть построены корреляционные диаграммы для гетероядерных двухатомных молекул. Несколько сложнее для двухатомных молекул построить корреляционные диаграммы для уровней полной электронной энергии ( без учета межъядерного отталкивания), прежде всего по той причине, что требуемая информация об электронных состояниях атомов, как правило, более скудна, чем для орбиталей. [33]
 |
Номенклатура силовых постоянных. [34] |
Процедура построения потенциальной функции молекулы набором указанных силовых постоянных не означает принятия какой-либо модели силового поля, она соответствует представлению функции разложением в ряд Тейлора и в этом смысле универсальна. Идея, положенная в основу теории силового поля Юри - Бредли, состоит в учете отталкивания валентно-несвязанных атомов, трактуемого как проявление Ван-дер-ваальсова взаимодействия. Z), что в конечном итоге должно было значительно сократить число подлежащих определению силовых постоянных. Неоднократные проверки на материале однозначно определенных потенциальных функций различных молекул показали, что в своем первоначальном виде модель Юри - Бредли не в состоянии правильно описать действительное силовое поле молекул. Модификация модели путем введения в нее в явном виде силовых постоянных типов AXYZ и / XYZW [18] сводит на нет ожидаемые преимущества, связанные с малым числом силовых постоянных, оставляя в силе недостатки, обусловленные весьма сложной процедурой построения потенциальной функции в естественных колебательных координатах. В связи с этим применение модели силового поля Юри - Бредли непосредственно в расчете колебаний молекул представляется нерациональным. [35]
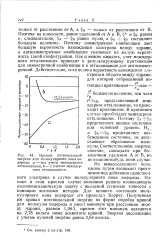 |
Кривые потенциальной энергии для молекулярного иона водорода. а - без учета межядерного отталкивания, Ь - с учетом межядерного отталкивания. [36] |
Поэтому на плоскости, равно удаленной от А и В, фА и фв равны и, следовательно, фд - фв равно нулю, а фА фв составляет большую величину. Поэтому симметричная комбинация дает большую вероятность нахождения электрона между ядрами, а антисимметричная комбинация указывает на малую вероятность такой конфигурации. Как и можно ожидать, учет межядер-ного отталкивания приводит к результирующему притяжению для симметричной комбинации и к отталкиванию для антисимметричной. [37]
Составляющую H dd обычно называют лондоновской дисперсионной силой. Физически эта сила связана с тем, что между мгновенной ориентацией дипольных моментов двух электронных облаков имеется корреляция. Наиболее выгодной является антипараллельная ориентация дипольных моментов, способствующая уменьшению полной энергии взаимодействия. Следовательно, эта сила всегда является притягивающей. Вычисления дисперсионных сил, проведенные для благородных газов [13], достаточно хорошо согласуются ( с учетом отталкивания ионных оболочек) с уравнением состояния разреженного газа и измеренными значениями вязкости. [38]
Теперь следует выяснить, как это взаимное влияние отражается на результатах. При этом необходимо принимать во внимание только электрическое взаимодействие. Магнитные силы между магнитными моментами, связанными со спинами электронов и их орбитальным вращением ( о чем до сих пор также не упоминалось в этой главе, хотя этот вопрос вкратце был рассмотрен в конце § 6.2), оказываются значительно меньше и ими можно пока пренебречь. Электрическая сила, которую мы хотим принять в расчет, является электростатическим взаимным отталкиванием электронов. Поскольку это так, следует считать, что энергия любого состояния с учетом отталкивания будет больше, чем получаемая при пренебрежении отталкиванием, однако точная величина энергии, на которую увеличивается при этом ф или ср, зависит от того, какая из возможных антисимметричных комбинаций рассматривается. Если волновая функция антисимметрична в спиновой части, то она симметрична в орбитальной части, и наоборот. [39]
Страницы: 1 2 3