Возникновение - положительный заряд
Cтраница 2
Поэтому существенной стадией, определяющей скорость катализируемой кислотой реакции присоединения, очевидно, является нуклеофильная атака галогена на ион, образующийся в результате протонирования группы, сопряженной с двойной связью. Благодаря сопряжению становится возможной делокализация заряда и возникновение положительного заряда на атоме углерода, атакуемом галогеном, как это показано в уравнении ( 7 - 8) на примере альдегида. [16]
Активные центры при катионной полимеризации появляются в результате возникновения положительного заряда у одного из углеродных атомов молекулы мономера. Например, полимеризация изобутилена в присутствии фторида бора и при участии ( в качестве сокатали-затора) воды протекает следующим образом. [17]
Наиболее равномерное распределение Ni2 no глубине гранул носителя наблюдается для хлорида никеля: для - образования наружной оболочки на гранулах носителя, предпочтительным оказывается сульфат никеля. При уменьшении рН раствора количество ионов никеля, равновесно адсорбированного на А12О3, уменьшается из-за возникновения положительного заряда на поверхности носителя. [18]
Наиболее равномерное распределение Ni2 по глубине гранул носителя наблюдается для хлорида никеля; для образования наружной оболочки на гранулах носителя предпочтительным оказывается сульфат никеля. При уменьшении рН раствора количество ионов никеля, равновесно адсорбированного на А12О3, уменьшается из-за возникновения положительного заряда на поверхности носителя. [19]
Наряду с этим типом, большое значение имеют донорно-ак-цепторные связи, образующиеся за счет пары электронов одного атома и свободной вакантной орбитали другого. В то же время ее переход в общее владение двух атомов означает передачу акцептору дополнительного отрицательного заряда и возникновение положительного заряда на доноре. [20]
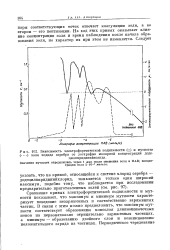 |
Зависимость электрофоретической подвижности ( О и мутности. [21] |
Сравнение кривых электрофоретической подвижности и мутности показывает, что максимум и минимум мутности характеризует поведение незаряженных и соответственно заряженных частиц. В связи с этим можно предположить, что максимум мутности соответствует образованию монослоя длинноцепочечных ионов на первоначально отрицательно заряженных частицахт а минимум - образованию двойного слоя и возникновению положительного заряда на частицах. [22]
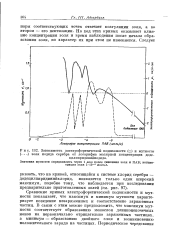 |
Зависимость электрофоретической подвижности ( о и мутности. [23] |
Сравнение кривых электрофоретической подвижности и мутности показывает, что максимум и минимум мутности характеризует поведение незаряженных и соответственно заряженных частиц. В связи с этим можно предположить, что максимум мутности соответствует образованию монослоя длинноцепочечных ионов на первоначально отрицательно заряженных частицах, а минимум - образованию двойного слоя и возникновению положительного заряда на частицах. [24]
 |
Спектр поглощения аитрахинона ( в диоксаве.| Молекулярная диаграмма антрахинона. а - основное состояние. б - возбужденное состояние. [25] |
На рис. 36 приведены молекулярные диаграммы антрахинона в основном ( а) и первом синглетиом возбужденном ( б) состояниях, составленные по данным квантово-химических расчетов по методу МО ССП. Вычисленные значения я-электронных порядков связей свидетельствуют о высокой выравненное связей в основном состоянии в обоих бензольных кольцах: я-составляющие связей колеблются в пределах 0 649 - 0 669, за исключением связей между атомами 4а - 9а и 8а - 10а, я-составляющие которых понижены до 0 599 взаимодействием с соседними карбонильными группами. Это же взаимодействие ( оттягивание электронов) обусловливает возникновение положительных зарядов на а - ( 1, 4, 5, 8) и р-углеродных атомах ( 2, 3, 6, 7) антрахинона, дезактивирующих молекулу в реакциях электрофильного замещения. [26]
Но атом кислорода, связанный двойной связью, оттягивает электроны от атома углерода. Этот атом, в свою очередь, оказывает такие же воздействие на гидроксильный кислород, так что в результате у последнего остается положительный заряд. Благодаря этому протон отталкивается, что и приводит к увеличению константы кислотности вследствие индуктивного эффекта. Еще более существенным фактором в возникновении положительного заряда у гидроксильного кислорода является резонанс со структурой В. Высокая кислотность карбоксильной группы в основном может быть приписана этому эффекту. [27]
Осаждение белков солями тяжелых металлов ( в отличие от высаливания) происходит при небольших концентрациях солей. Белки при взаимодействии с солями тяжелых металлов ( свинца, меди, серебра, ртути и др.) адсорбируют их, образуя с ними солеобразные и комплексные соединения, растворимые в избытке этих солей ( за исключением солей AgNO3, HgCl2), но нерастворимые в воде. Соли тяжелых металлов вызывают необратимое осаждение белков, т.е. денатурацию. Растворение осадка в избытке солей называется адсорбционной пептизацией. Данное явление происходит вследствие возникновения одноименного положительного заряда на частицах белка. [28]
Рассмотрим теперь сосуд ( рис. 3.3) с проводящей жидкостью, находящейся в состоянии турбулентного движения. Турбулентность должна быть однородной и изотропной, но иметь спиральность, т.е. один из видов спирального движения должен быть более вероятен, чем другой. Примем, например, что большую вероятность имеют лево-винтовые спиральные движения. Пусть магнитное поле В направлено слева направо. В этих условиях должен проявляться а-эффект и, следовательно, должно существовать электрическое поле параллельное магнитному полю. Оно приводит к возникновению положительного заряда на левой стенке сосуда и отрицательного - на правой. [30]
Страницы: 1 2
