Возникновение - молекула
Cтраница 2
Молекулярная ассоциация может быть обусловлена как электростатическим, так и диполь-дипольным взаимодействием между молекулами, входящими в состав ассоциата. Различные типы связи, обусловливающие возникновение молекулы ассоциата Аж, в том числе и наиболее часто встречающийся случай водородной связи ( Н - связи), могут быть в первом приближении сведены к этим типам взаимодействия. [16]
Вероятно, это связано с равновесием по схеме: ОС. Хотя оно и должно быть сильно смещено влево, существование его все же обеспечивает постоянную возможность временного возникновения неустойчивых молекул изохлорноватистой кислоты ( Н: С1: О:), структура которых позволяет предполагать наличие у них повышенной тенденции к отщеплению активного атома кислорода. [17]
Вероятно, это связано с равновесием по схеме: ОСГ НОС1 - ОС1Н ОСГ. Хотя оно и должно быть сильно смещено влево, его существование все же обеспечивает постоянную возможность временного возникновения неустойчивых молекул изохлорноватистой кислоты ( Н: С1: О:), структура которых позволяет предполагать наличие у них повышенной тенденции к отщеплению активного атома кислорода. [18]
Рассматривая пути появления вод в литосфере, следует отметить два источника возникновения молекул воды - экзогенный и эндогенный. Подземные воды, образующиеся в результате поступления вод в горные породы из внешних геосфер - гидросферы и атмосферы - экзогенные, а за счет возникновения молекул воды в недрах земли - эндогенные. Эндогенные воды формируются в горных породах и магматических очагах в результате различных химических реакций. [19]
Известно, что при взаимодействии излучения с веществом наряду с ионами образуются и возбужденные молекулы. При непосредственном действии налетающей заряженной частицы в среде возникают низшие энергетические состояния, аналогичные фотовозбуждению. Возникновение молекул высших степеней возбуждения происходит в [ результате захвата образовавшимся положительным ионом электрона либо непосредственно, либо в виде отрицательного иона. [20]
Имеется указание [10], что водный раствор бензидина дает также синюю поверхностную окраску, притом только для монтмориллонитов, что было предложено в качеств е пробы на этот минерал. Авторы, незнакомые с вышеуказанной литературой вопроса, предполагают, что эта окраска вызвана растворенными ионами Fe3, окисляющими бензидин в растворе, причем образующийся окрашенный семихинон адсорбируется из растворов. Наши опыты с несомненностью указывают на поверхностное возникновение окрашенных молекул. [21]
Точное определение связи между оптической активностью л молекулярной структурой было дано в классической работе Вант-Гоффа, относящейся к 1874 г. К такому же выводу в том же году пришел Ле-Бель. Ваит-Гофф заметил, что подавляющее большинство оптически активных веществ содержит асимметрически атом углерода. Он установил, что если атом углерода имеет тетраэдрический характер, то это обусловливает возникновение молекул, находящихся в энантиоморфных отношениях. Вант-Гофф высказал также предположение о других типах молекул, которые, вероятно, могут находиться в оптически активной форме. Трудно переоценить значение стереохи-мических работ Вант-Гоффа. Большинство исследований оптической изомерии, проведенных в последующие 75 лет, служили только с большим или меньшим изяществом подтверждением справедливости теории Вант-Гоффа. Вероятно, наиболее убедительное доказательство могущества идеи Вант-Гоффа было дано исследованиями Эмиля Фишера в ряду углеводов. Как указал Вант-Гофф, соединение, содержащее п асимметрических атомов углерода, должно существовать ( если исключена возможность внутренней компенсации) в 2п оптически активных формах. [22]
Оси порядка выше шести исключаются, поскольку они запрещены симметрией кристаллической решетки. Действительно, если бы молекула занимала частное положение, то элемент симметрии пространственной группы являлся бы элементом симметрии ее точечной группы, а значит, она являлась бы лгезо-формой и не была бы асимметричной. Если бы молекула занимала общее положение, то элементы симметрии пространственной группы привели бы к возникновению энантио-морфной молекулы, в результате чего должен был бы образоваться рацемат. Это означает, что из 230 пространственных групп только 65 являются допустимыми для кристаллизации оптически активных веществ. Автор не может отыскать ни одного исключения из этого правила. Если бы оно было обнаружено ( а это не кажется невероятным), то естественно было бы объяснить его неупорядоченностью структуры, например вращением молекул в кристалле; при этом молекула может имитировать симметрию более высокую, чем ее собственная ( см. стр. [23]
Порядок связи равен частному от деления разности числа электронов на СМО и РМО на число взаимодействующих атомов. Порядок связи может принимать и целочисленные, и дробные значения, но только положительные. Если порядок связи равен нулю, система неустойчива и связь не возникает. Это значит, что для возникновения молекулы или любой многоатомной системы необходимо, чтобы заселенность электронами СМО была всегда больше, чем заселенность РМО. Тогда образующаяся система энергетически выгодна и стабильно существует. Порядок связи в ММО есть, по существу, превращенная форма понятия валентности классической химии, кратности связи в МВС. Нецелочисленные же значения порядка связи - прямое следствие многоцентровости и делокатщзации связей в методе МО. [24]
Порядок связи равен частному от деления разности числа электронов на СМО и РМО на число взаимодействующих атомов. Порядок связи может принимать и целочисленные, и дробные значения, но только положительные. Если порядок связи равен нулю, система неустойчива и связь не возникает. Это значит, что для возникновения молекулы или любой многоатомной системы необходимо, чтобы заселенность электронами СМО была всегда больше, чем заселенность РМО. Тогда образующаяся система энергетически выгодна и стабильно существует. Порядок связи в ММО есть, по существу, превращенная форма понятия валентности классической химии, кратности связи в МВС. Нецелочисленные же значения порядка связи - прямое следствие многоцентровости и делокализации связей в методе МО. [25]
 |
Схема неравновесных энергетических состояний в полупроводнике и физический механизм образования электронно-дырочной жидкости. [26] |
Система свободных носителей в полупроводниках при высоких темп - pax представляет собой слабо неидеальную, полностью ионизованную плазму. При низких темп-рах и высоких концентрациях носителей я, когда П в 1 ( ое-10 - 6 - н10 7 см-боровский радиус экситона), она приобретает свойства вырожденного ферми-газа. Sei - 10 1 - 10 эВ - энергия связи экситона), электронно-дырочные пары ( ЭДП) связываются в экситоны и образуют атомарный газ. При еще более низких темп - pax возможно возникновение экситон-ных молекул, или бижситопов, с очень малой энергией связи. Необычные коллективные явления возникают в этой системе при низких темп - pax и относительно высоких концентрациях. [27]
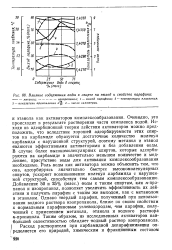 |
Влияние содержания воды в спирте на выход и свойства парафина. [28] |
Очевидно, это происходит в результате растворения части комплекса водой. Исходя из адсорбционной теории действия активаторов можно предположить, что вследствие хорошей адсорбируемости этих спиртов на карбамиде образуется достаточное количество молекул карбамида с нарушенной структурой, поэтому метанол и этанол являются эффективными активаторами и без добавления воды. В - случае более высокомолекулярных спиртов, которые адсорбируются на карбамиде в значительно меньшем количестве и медленнее, присутствие воды для активации комллексообразования необходимо. Роль воды как активатора можно объяснить тем, что она, адсорбируясь значительно быстрее высокомолекулярных спиртов, ускоряет возникновение молекул карбамида с нарушенной структурой, способствуя тем самым комплексообразованию. Добавление 50 и 25 % ( масс.) воды к таким спиртам, как м-про-панол и изопропанол, позволяет увеличить эффективность их действия и получить парафин с таким же выходом, как - с метанолом и этанолом. Однако твердый парафин, полученный при использовании водного раствора изопропанола, ближе по своим свойствам к ормальным парафиновым углеводородам, чем парафин, полученный с применением метанола, этанола и водного раствора - пропанола. Таким образом, из исследованных активаторов наибольшей селективностью обладает водный раствор изопропанола. [29]
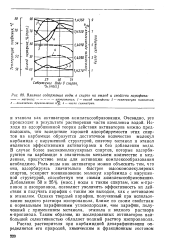 |
Влияние содержания воды в спирте на выход и свойства парафина. [30] |
Страницы: 1 2 3