Возникновение - радикал
Cтраница 3
На примерах радикалов, образующихся при воздействии излучения на пальмитивную кислоту, трипальми-тин и пальмитат кальция Бах и Ревина [40, 41] установили, что возникновению радикалов RO2 предшествует образование малоустойчивого непарамагнитного соединения. [31]
Имеются случаи, когда свободным радикалом является ион, например ион Na - бирадикал, тогда сам первичный процесс ионизации электронным ударом ведет к возникновению радикала. Вообще специфичность химического действия электрических разрядов эти авторы видят в том, что энергия, подводимая к разряду, в первой стадии своего превращения концентрируется в электронном газе. При этом в связи с большим различием масс электронов и молекул, передача энергии путем упругих столкновений от электронов к молекулам происходит медленно. [32]
Хотя много вопросов остается выяснить в дальнейших опытах, тем не менее это антистоксово излучение, возникающее вдоль лазерного пучка, не может быть объяснено возникновением радикалов или ион-радикалов с последующей их излучательной рекомбинацией, так как фталоцианины, которые известны как очень близкие фотохимические аналоги хлорофилла и его производных, не дают подобного антистоксова излучения. [33]
Условно к разветвленным цепным реакциям можно отнести реакции окисления углеводородов, поскольку здесь при развитии цепи образуются перекиси и альдегиды, которые гораздо легче могут приводить к возникновению радикалов, чем исходные вещества. Это объясняет наличие длинных периодов индукции и начального автоускорения реакции, а также явления нижнего предела реакции. Эти явления определяются возможностью или невозможностью нарастания концентрации этих промежуточных продуктов, например конкуренцией между мономолекулярным распадом перекиси на радикалы и бимолекулярным процессом прямого их распада на молекулы при соударении двух молекул перекиси. [34]
Параметры сигнала ЭПР от перекисных центров также приведены в табл. 4.1. Флори и Девине [59], исследуя ранние стадии окисления атомарно-чистых поверхностей кремния методом ЭОС, также допускают возможность возникновения радикалов. Стерн и Хюбнер [60] считают, что в SiO2 и в граничной фазе Si - SiO2 могут образовываться три ( Оз) - и одно ( ОГ) координированные парные кислородные дефокхы. В случае Oj третья ( более слабая) связь Si - О образуется зг счет неподеленной нары электронов кислорода. [35]
Таковы современные схемы гомогенного окисления углеводородов, в которых главную роль играют перекисные радикалы, способные изомеризоваться, и распад которых приводит к образованию всех стабильных кислородсодержащих продуктов, обнаруженных при окислении пропилена и пропана. Возникновение радикалов облегчает протекание окислительной реакции. [36]
Этот разрыв, независимо от вызвавших его причин, приводит к появлению свободных радикалов на концах разорванной цепи. Возникновение радикалов вызывает ряд вторичных процессов. Такими процессами являются приводящее к образованию разветвленных цепей взаимодействие радикалов с цепными молекулами, инициирование окислительных процессов ( дальнейшее развитие которых протекает в соответствии с химической спецификой полимера), гашение радикалов в результате их взаимодействия с образующими насыщенные соединения веществами. [37]
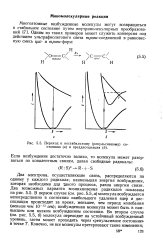 |
Переход к нестабильному ( репульсивному состоянию ( а и преддисоциация ( б. [38] |
Два электрона, осуществляющие связь, распределяются по одному у каждого радикала; наименьшая энергия возбуждения, которая необходима для такого процесса, равна энергии связи. Два возможных варианта возникновения радикалов показаны на рис. 5.5. В первом случае ( см. рис. 5.5, а) молекула возбуждается непосредственно в состоянии наибольшего удаления ядер и диссоциация происходит за время, меньшее, чем период колебания ( меньше чем 10 - 13 сек); возбужденная молекула может быть в наивысшем или низком возбужденном состоянии. [39]
Детар и Вейсс [32] нашли, что при разложении перекиси Р - фенилизобутирила в четыреххлористом углероде, 1-фенил - 2-пропанол, который получается из образующегося в ходе реакции эфира, на 75 % сохраняет первоначальную конфигурацию перекиси. Исследователи объясняют это возникновением радикалов в одной клетке растворителя, которые затем реагируют с образованием эфира быстрее, чем 1-фенил - 2-пропильный радикал может изменить ориентацию по отношению к карбоксильному радикалу. [40]
 |
Окисление углеводородов кислородом и окисью азота. [41] |
Результаты изучения гетерогенно-гамогенных процессов в газовой фазе показали, что некоторые продукты мягкого окисления углеводородов образуются не на поверхности, а в объеме. Эти данные указывают на возникновение радикалов на поверхности катализаторов, что подтверждено экспериментально методом ЭПР для окисления метана. [42]
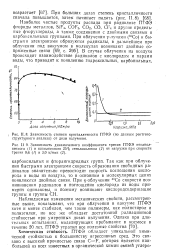 |
Зависимость степени кристалличности ПТФЭ ( по данным рентгено-структурного анализа от дозы излучения. [43] |
Так как при облучении быстрыми электронами скорость образования свободных радикалов значительно превосходит скорость поглощения кислорода и воды из воздуха, то в основном в молекулярных цепях появляются двойные связи. При у-облучении 60Со скорости возникновения радикалов и поглощения кислорода из воды примерно одинаковы, и поэтому возникают кислородсодержащие группы и группы СН. [44]
Взаимодействие других органических веществ с молекулярным кислородом при облучении также происходит по цепному механизму. Первичным процессом здесь тоже является возникновение радикала, который затем образует перекисный радикал. [45]
Страницы: 1 2 3 4