Изучение - скорость - химическая реакция
Cтраница 2
Первоначально при изучении электрохимической кинетики использовали те же приемы, что и при изучении скорости химических реакций. [16]
Химические реакции протекают с определенными скоростями. Изучением скоростей искусственных химических реакций занимается физическая химия, а скоростей природных химических реакций - физическая геохимия. [17]
 |
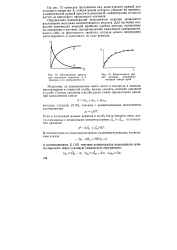
Кинетические кривые для исходного вещества А и продукта его превращения В. [18] |
Определение концентраций компонентов реакции проводится различными методами количественного анализа. Для изучения скоростей химических реакций наиболее удобны методы, основанные на измерении в системе, претерпевающей химическое превращение, какого-либо физического свойства системы, которое можно непрерывно регистрировать и записывать по ходу реакции. [19]
 |
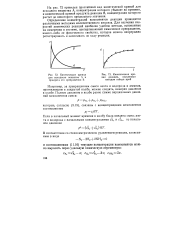
Кинетические кривые.| Кинетическая кривая реакции, полученная методом отбора проб. [20] |
Определение концентраций компонентов реакции проводится различными методами количественного анализа. Для изучения скоростей химических реакций наиболее удобны методы, основанные на измерении в системе, претерпевающей химическое превращение, какого-либо ее физического свойства, которое можно непрерывно регистрировать и записывать по ходу реакции. [21]
 |
Кинетические кривые.| Кинетическая кривая реакции, полученная методом отбора проб. [22] |
Определение концентраций компонентов реакции проводится различными методами количественного анализа. Для изучения скоростей химических реакций наиболее удобны методы, основанные на измерении в системе, претерпевающей химическое превращение, какого-либо ее физического свойства, которое можно непрерывно регистрировать и записывать по ходу реакции. [23]
Концентрацией называют количество растворенного вещества, содержащееся в определенном количестве раствора. При изучении скорости химических реакций концентрации обычно выражают числом грамм-молекул вещества, содержащихся в 1 л раствора 1 а время - в секундах, минутах и часах, в зависимости от величины скорости реакции. [24]
Концентрацией называют количество растворенного вещества, содержащееся в определенном количестве раствора. При изучении скорости химических реакций концентрации обычно выражают числом грамм-молекул вещества, содержащихся в 1 л раствора 1 а время в секундах, минутах и часах в зависимости от величины скорости реакции. [25]
Концентрацией называют весовое или объемное количество растворенного вещества, содержащееся в определенном количестве раствора. При изучении скоростей химических реакций концентрации обычно выражают числом грамм-молекул вещества, содержащихся в 1 л раствора, J а время - в минутах. [26]
Так как любое химическое превращение ведет систему к состоянию равновесия, то всякую химическую реакцию можно рассматривать в качестве релаксационного процесса. В настоящее время разработаны многие методы изучения скоростей химических реакций, которые так и называются релаксационными. Примером может служить изучение рекомбинации ионов иода в растворе. Раствор иода, например, в че-тыреххлористом углероде освещают кратковременной вспышкой импульсной лампы. При этом происходит диссоциация молекул иода на свободные атомы, которые в растворе в отличие от молекул не поглощают видимого света. Местные релаксационные процессы постоянно происходят при различного рода флуктуациях, а также, например, при прохождении звука через среду, что связано с местными адиабатическими сжатиями. [27]
Из (11.14) видно, как можно экспериментально определить скорость химической реакции по какому-либо компоненту. Зависимость c ( t) при изучении скоростей химических реакций часто изображают графически и называют получающуюся линию кинетической кривой реакции. Функциональную зависимость c ( t) называют уравнением кинетической кривой. [28]
Последнее обстоятельство позволяет без труда получать расчетные формулы для сравнительно сложных случаев реакций. Наличие подобных формул является необходимой предпосылкой для изучения скорости химических реакций. [29]
Превращения элементов на различных стадиях происходят с различной интенсивностью. Интенсивность радиоактивного распада подчиняется закону, который мы подробно рассмотрим при изучении скорости химических реакций ( гл. [30]
Страницы: 1 2 3