Изучение - первичная структура
Cтраница 2
Хотя дисульфидные связи частично обусловливают вторичную и третичную структуры белков, определение их локализации является частью изучения первичной структуры. [16]
Таким образом, ДНК у анаэробов имеет интересные особенности, и очень многого можно ожидать в будущем от изучения первичной структуры ДНК этих бактерий. [17]
Весьма перспективны такие ферменты микроорганизмов, как холестеринок-сидаза, для определения холестерина в крови, алкогольоксидаза для обнаружения спирта и др. Ферменты используют также для изучения первичной структуры высокомолекулярных соединений: нуклеиновых кислот, белков, полисахаридов. [18]
Фракционирование сложных смесей веществ является одним из основных этапов в решении многочисленных проблем биохимии, биофизики и молекулярной биологии, в связи с тем что биологические системы содержат большое число компонентов, часто близких по ряду химических и физических свойств, а также в связи с развитием методов изучения первичной структуры биополимеров. Выделение отдельных компонентов из таких систем является, как правило, весьма сложной экспериментальной задачей, решение которой ранее осуществлялось путем использования физико-химических методов - осаждения, кристаллизации и сорбции. В настоящее время имеется большой арсенал средств избирательного выделения компонентов или разделения сложных смесей с получением всех веществ в чистом виде. К ним относятся в области изучения биополимеров и их фрагментов прежде всего хроматография и электрофорез. Для аналитических целей при рассмотрении систем, содержащих ограниченное число компонентов, успешно применяется также седиментация, диффузия и ряд других процессов, в которых осуществляется обычно не полное разделение компонентов, а относительное смещение границ зон отдельных веществ. [19]
Как 15 -, так и 55-членный пептид не содержит гистидина, и, таким образом, необходимая имидазольная группа оказывается вблизи серина в результате скручивания белка. Очень близкая картина наблюдается и в случае химотрипсина, как было показано в работах Хартли [1] по изучению первичной структуры химотрипсина. [20]
Полипептидные цепи можно избирательно разрушить по остаткам метионина с помощью бромциана. Разумеется, анализ полученной смеси не позволит восстановить последовательность фрагментов в исходной полипептидной цепи. Однако такого рода избирательное расщепление оказывает существенную помощь в изучении первичной структуры. [21]
N - и С-концевыми методами чередование в них аминокислотных остатков Применяя различные способы частичного гидролиза, устанавливают строение большого числа различных пептидных фрагментов, затем находят тождественные ( перекрывающиеся) участки этих пептидов, по этим данным устанавливают последовательность расположения остатков в исходной цепи. Полипептидную цепь, состоящую из большого числа ( более 150 - 200) остатков, предварительно подвергают Селективному гидролизу на несколько частей ( напр. Локализацию диеуль-фидных связей устанавливают частичным ( обычно ферментативным) гидролизом, выделением пептидов с дисульфидными связями и разрывом этих связей окислением ( напр, надмуравьиной к-той), каждую образующуюся пару пептидов с сульфогруппами цистеиновой к-ты разделяют, устанавливают строение пептидов и находят их места в уже расшифрованной полипептидной цепи. Как уже отмечалось, при изучении первичной структуры пользуются N - и С-концевыми методами, позволяющими установить природу остатка аминокислоты, находящегося на N-конце и С-конце полипептидной цепи со свободными группами a - NH2 и a - СООН соответственно. [22]
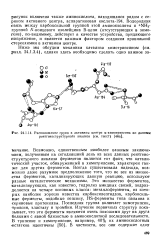 |
Расположение групп в активном центре ос-химотрипсина по данным рентгеноструктурного анализа ( текст [ 46а ]. [23] |
Возможно, единственным наиболее важным заключением, полученным на сегодняшний день из всех данных рентгеноструктурного анализа ферментов является тот факт, что каталитический участок, обнаруженный в химотрипсине, характерен также для других ферментов. Всегда существовала надежда, возможно даже разумное предположение того, что не все из множества ферментов, катализирующих данную реакцию, используют разные каталитические механизмы. Это множество ферментов, катализирующих, как известно, гидролиз амидных связей, подразделяется на четыре основных класса: металлоферменты, из которых наиболее хорошо известна карбоксипептидаза, карбоксильные ферменты, подобные пепсину, HS-ферменты типа папаина и сериновые протеиназы. Последняя группа включает химотрипсин, трипсин, эластазу и тромбин. Изучение первичных структур показывает, что эти ферменты являются очень похожими друг на друга белками с явной близостью в аминокислотной последовательности. [24]
Примен ш различные способы частичного гидролиза, устанавливают строение большого числа различных пептидных фрагментов, затем находят тождественные ( перекрывающиеся) участки эт. Полппептидную цепь, состоящую из большого числа ( более 150 - 200) остатков, предварительно подвергают селективному гидролизу на несколько частей ( напр. Локализацию дисуль-фидных связей устанавливают частичным ( обычно ферментативным) гидролизом, выделением пептидов с дисульфидными связями и разрывом этих связей окислением ( напр. Как уже отмечалось, при изучении первичной структуры пользуются N - и С-концевыми методами, позволяющими установить природу остатка аминокислоты, находящегося на N-конце и Оконце полипептидной цепи со свободными группами oc - NlI2 и сс - СООН соответственно. [25]
Страницы: 1 2