Возрастание - концентрация - электролит
Cтраница 3
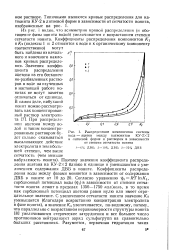 |
Распределение компонентов системы. [31] |
Поэтому значения коэффициента распределения ацетона на КУ-2 X 2 близко к единице и уменьшаются с увеличением содержания ДВБ в ионите. Согласно уравнению ty1 RT nKi, сорбционный потенциал воды ( ifi) в зависимости от степени сетчатости ионита лежит в пределах 1350 - 1750 кал / моль, в то время как сорбционный потенциал ацетона равен нулю или имеет отрицательное значение. С увеличением сетчатости ионита значение Къ уменьшается ( благодаря возрастанию концентрации электролита в фазе ионита), а значение / d увеличивается, по-видимому, потому, что параллельно с возрастанием неравномерности структуры ионита [8] увеличиваются стерические затруднения и все большее число противоионов нейтрализует заряд сульфогрупп на сравнительно больших расстояниях. [32]
Концентрационная зависимость коэффициентов диффузии, обусловленная связыванием электролита ионогенными группами полимера. Наиболее подробно концентрационная зависимость коэффициентов диффузии изучена при сорбции кислот полиамидами. В работах [125-129, 136] установлено значительное увеличение коэффициентов диффузии с возрастанием концентрации электролита в растворе. [33]
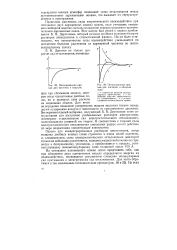 |
Потенциальная кривая для частичек в вакууме.| Потенциальные кривые для частичек в обычном золе. [34] |
Экспериментальный материал, полученный Б. В. Дерягиным и его сотрудниками для достаточно разбавленных растворов электролитов, подтвердил существование сил электростатического отталкивания, подчиняющихся развитой им теории. В соответствии с теорией силы электростатического отталкивания уменьшают радиус свсего действия по мере возрастания концентрации электролита. [35]
Когда же проводились опыты с заполнением прибора И. И. Жукова и А. А. Крюкова каждый раз заново с данной концентрацией раствора или велись опыты параллельно по методике фильтрационного анализа, в этих случаях скорость фильтрации изменялась. Очевидно, что наблюдающиеся изменения в скорости фильтрации в этих случаях связаны с процессами агрегации и коагуляции частиц. Это подтверждают также наблюдения за изменением объема осадка, который значительно увеличи-вался при возрастании концентрации электролита, и результаты по промывке осадков водой без механического нарушения структуры. [36]
Радиохимические количества таких нерастворимых металлов, как цирконий, ниобий или протактиний, могут в значительной степени адсорбироваться катио-нитами. В противоположность адсорбции катионов, адсорбция коллоидных веществ в радиохимических концентрациях - радиоколлоидов - остается неизменной или даже увеличивается с возрастанием концентрации несущего электролита. Последний может действовать в данном случае в качестве коагулятора и усиливать тем самым адсорбцию радиоколлоида. [37]
Дальнейшее повышение концентрации электролита, как это было показано на примере водного раствора хлорида натрия, приводит к некоторому замедлению спада диэлектрической постоянной и отклонению экспериментальной кривой от прямой линии в сторону больших величин диэлектрической постоянной. Предполагается, что такой ход кривых D - с обусловлен наложением эффектов упорядочения структуры воды и ее разрушения под действием введенных ионов. Если рассматривать воду как систему, состоящую из квазикристаллических образований, распределенных в аморфной жидкости, то при введении первых порций электролита наиболее заметно проявляются их упорядочивающее действие - образование внутреннего сольватного ( замороженного) слоя молекул воды, частичная ориелтация молекул воды во внешнем сольватном слое; уменьшение свободного объема жидкости. Все эти эффекты охватывают главным образом преобладающую аморфную форму воды, связь между молекулами в которой ниже, чем в квазикристаллических образованиях, и приводят к уменьшению энтропии. При возрастании концентрации электролита, когда значительная часть аморфной воды уже связана, в формирование гидратных оболочек вовлекаются квазикристаллические образования, их упорядоченность снижается, а энтропия возрастает. [38]
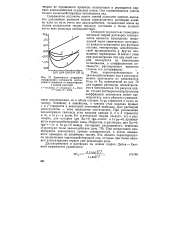 |
Зависимость логарифма коэффициента активности растворенного вещества от концентрации. [39] |
Из рисунка видно, что для растворов неэлектролитов коэффициент активности может как возрастать, так и убывать с уменьшением концентрации, но в обоих случаях 1пув стремится к нулю по закону, близкому к линейному, а тангенс угла наклона кривых 1 и 2 стремится к некоторой, постоянной величине. При уменьшении концентрации тангенсы угла наклона кривых 3, 4 и 5 стремятся к оо, a In Y - к нулю. Из статической теории следует, что в растворах, для которых при Хв - э - 0 tga - K: onst и In ув-0, проявляются короткодействующие силы. При возрастании концентрации электролита кривые сглаживаются, а затем изменяются-примерно по линейному закону. Эта область характеризуется проявлением короткодействующих сил, которые при более высоких концентрациях играют уже решающую роль. [40]
Особый интерес представляют вторичные черные пленки, механизм устойчивости которых не ясен. Результаты, полученные в работах [ 1J и [6], интерпретируются в том смысле, что черные пленки не содержат или почти не содержат воды. Очень тщательные измерения толщины были проведены в работе [7] в комбинации с прямым измерением содержания йоды ( по абсорбции ИК-света) на черных пленках из растворов алкилтри-метиламониевых алкилсульфатов. Полагая, что черные пленки имеют трехслойную структуру ( два плотных адсорбционных слоя ПАВ, разделенных прослойкой из водного раствора - так называемая сандвич-модель), авторы определяют толщину водной прослойки от 20 до 50 А для различных измеренных ими пленок. В этой работе, к сожалению, нет указаний на то, к какому из двух видов черных пленок относятся измеренные объекты. Можно лишь предполагать, что наименьшее значение в 20 А, являющееся асимптотическим при возрастании концентрации электролита, действительно относится к вторичным черным пленкам. [41]
Страницы: 1 2 3