Возрастание - число - атом
Cтраница 1
Возрастание числа атомов сверх восьми слабо влияет на ширину и форму зон уровней. Принципиальным эффектом является значительное возрастание плотности уровней в зонах. Ширина зон полностью зависит от силы взаимодействия. [1]
С возрастанием числа атомов фтора уменьшаются токсичность фреонов и реакционноспособность их к металлам и уплотняющим материалам, снижается растворимость в смазочных маслах и воде, увеличивается химическая стабильность. [2]
С возрастанием числа атомов F уменьшается токсичность, реакционная способность к металлам и уплотняющим материалам, снижается растворимость в смазочных маслах и воде, увеличивается химическая стабильность. С уменьшением числа атомов Н резко снижается воспламеняемость; фреоны без атомов водорода не горючи и в смеси с воздухом не воспламеняются. С увеличением числа атомов С1 повышается нормальная температура кипения фреонов. [3]
С возрастанием числа атомов углерода в цепи частоты лишь немного смещаются, да и то только у низших членов ряда; у высших членов они приближаются к некоторому предельному значению. [4]
При возрастании числа атомов азота в циклической системе реакции электрофильного замещения по С-атому ядра затрудняются, поэтому не удивительно, что в литературе такие реакции мало освещены. [5]
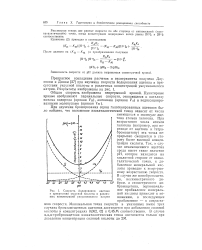 |
Скорость йодирования ацетона в присутствии уксусной кислоты и различных концентраций уксуснокислого натрия. [6] |
При возрастании числа атомов галогена ( например, при переходе от ацетона к тетра-бромацетону) эта точка непрерывно смещается в сторону более высокой концентрации кислоты. Так, в случае незамещенного ацетона среда имеет такое значение рН, которое находится на кислотной стороне от изокаталитической точки, и добавление минеральной кислоты приводит к непрерывному возрастанию скорости. В случае же монобромацетона, несимметричного ди-бром - и симметричного ди-бромацетона, первоначальное прибавление минеральной кислоты приводит к понижению, а последующее прибавление - к возрастанию скорости. Минимальная точка скорости в указанных выше трех случаях бромзам ещенных ацетонов достигается при добавлении соляной кислоты в концентрациях 0 002, 02 и 0 45 М соответственно. [7]
При возрастании числа атомов азота в циклической системе реакции электрофильного замещения по С-атому ядра затрудняются, поэтому не удивительно, что в литературе такие реакции мало освещены. [8]
По мере возрастания числа атомов в цикле увеличивается возможность осуществления в них более выгодных скошенных и заторможенных конформаций. Однако рассмотрение колец с числом ато-моз углерода от 7 до 12 показывает, что в них все же должны присутствовать и невыгодные группировки. В ряду циклов от трехчленного до двенадцатичленного исключение составляет лишь циклогек-сан, одна из конформаций которого ( стр. Это следует как из геометрических соображений, так и из термохимических данных. [9]
По мере возрастания числа атомов в цикле увеличивается возможность осуществления в них более выгодных скошенных и заторможенных конформации. Однако рассмотрение колец с числом атомов углерода от 7 до 12 показывает, что в них все же должны присутствовать и невыгодные группировки. В ряду циклов от трехчленного до двенадцатичлепиого исключение составляет лишь циклогек-саи, одна из конформации которого ( стр. Это следует как из геометрических соображений, так и из термохимических данных. [10]
Рассмотрим в порядке возрастания числа атомов в парамагнитной частице с одним неспаренным электроном некоторые достаточно простые радикальные системы. Ряд интересных проблем возникает при использовании спектров ЭПР в исследованиях двухатомных радикалов типа АН и АВ, позволяющих проверить современные представления об их электронном строении. Определены компоненты тензоров - фактора и сверхтонкого взаимодействия гидроксильного радикала ОН и ион-радикала NH в разных средах, характеризующие распределение электронной и спиновой плотности. [11]
Органические соединения даны в порядке возрастания числа атомов углерода, водорода, а затем других элементов в суммарной формуле соединения. Последовательность соединений с одинаковым числом атомов углерода и водорода определяется положением других элементов в периодической системе. [12]
Вещества расположены в таблицах по возрастанию числа атомов углерода, затем водорода и далее хлора. Все значения приведены в системах единиц СИ и МКС. [13]
Соединения в таблице расположены в порядке возрастания числа атомов углерода и водорода. В скобках приведены недостаточно падежные данные. [14]
Соединения расположены по брутто-формулам в порядке возрастания числа атомов углерода, водорода, брома, хлора, фтора, азота, кислорода, серы. При одинаковых брутто-формулах вначале помещены соединения нормального, а затем изо - и циклического строения. [15]
Страницы: 1 2 3 4