Возрастание - энтропия - система
Cтраница 1
Возрастание энтропии системы связано с тем, что энтропия рабочего тела за цикл не изменяется, а уменьшение энтропии горячих источников меньше по абсолютной величине, чем увеличение энтропии холодных источников тепла. Таким образом, в результате осуществления необратимого цикла энтропия изолированной системы возрастает. [1]
Проанализируем принцип возрастания энтропии системы, в которой происходят действительные ( необратимые) процессы, на нескольких примерах. Допустим, что в изолированной системе, состоящей из двух тел с постоянными температурами Т и Т2, причем TIT %, происходит переход тепла q от одного тела к другому. Допустим также, что температуры тел при переходе тепла остаются неизменными. [2]
Они сопровождаются возрастанием энтропии системы ( см. кинетика физ. [3]
 |
К производству энтропии при передаче тепла по стержню. [4] |
Заметим, что возрастание энтропии системы Y должно быть связано с присущей ей необратимостью, так как эта система является изолированной и через ее границу тепло не переносится. Однако необратимость в системе Y связана лишь со стержнем, ибо, по определению, процессы, протекающие в тепловом резервуаре, не могут быть необратимыми. [5]
В случае адиабатного процесса возрастание энтропии системы вызывается следующими двумя причинами: 1) необратимостью процесса парообразования при конечной разности температур между парогазовой смесью-и жидкостью и 2) необратимостью процесса смешения пара с влажным газом. [6]
Образованию хелата благоприятствует в основном возрастание энтропии системы ( ср. [7]
Здесь dS - общая скорость возрастания энтропии системы; diS - скорость, зависящая от внутренних процессов; deS - скорость, зависящая от процессов взаимодействия с внешней средой. [8]
 |
Термодинамические сорбции антибиотиков. [9] |
Обычно сорбция сложных органических ионов сопровождается возрастанием энтропии системы. Вторая отличительная особенность, проявляющаяся при высокой специфичности сорбции органических ионов, состоит в кооперативном эффекте взаимодействия противоионов на сорбенте, продемонстрированная на рис. 2 сорбцией окситетрациклина на макросетчатом сульфокатионите. [10]
 |
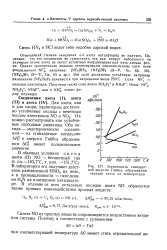
Зависимость стандартной энергии Гиббса образования оксидов азота от температуры. [11] |
Синтез NO из простых веществ сопровождается возрастанием энтропии системы. [12]
Синтез N0 из простых веществ сопровождается возрастанием энтропии системы. При этих, условиях начинает; доминировать энтропийный фактор. [13]
 |
Зависимость стандартной энергии Гиббса образования оксидов азота от температуры. [14] |
Синтез NO из простых веществ сопровождается возрастанием энтропии системы. [15]
Страницы: 1 2 3 4