Изучение - адсорбция - водород
Cтраница 1
Изучение адсорбции водорода на Ni, Co, Ni - Р и Со - Р электродах в присутствии органических добавок, Отч. [1]
 |
Гидрирование тиофена над субсульфидом никеля.| Гидрирование тиофена на смешанном окисно-дисуль-фидном молибденовом катализаторе. [2] |
Изучение адсорбции водорода, тиофена и тетрагидротиофена показало, что на двусернистом молибдене водород адсорбируется значительно сильнее, чем тиофен; на смешанном катализаторе наблюдалось обратное явление. [3]
Проведено изучение адсорбции водорода методом термодесорбции и сравнительная гидрогенизация соединений различной адсорбционной способности на никель-хромовых, палладиевых, платино-палладиевых, палладий-родиевых катализаторах на носителях. Показано, что формы адсорбированного водорода, энергия связи Н - К предопределяют активность, избирательность и стабильность металлических контактов при гидрогенизации различных типов органических соединений. Степень участия в катализе различных форм адсорбированного водорода и степень их воспроизводства определяются адсорбционной способностью органического соединения, природой растворителя и величиной удельной поверхности, на которой адсорбируется активная форма водорода. [4]
При изучении адсорбции водорода на пироуглероде установлено, что количество электричества ( Q), найденное интегрированием /, р-кривых, зависит от скорости ( и) наложения потенциала. [5]
Более интересны работы Дзидзима [7] по изучению адсорбции водорода на никеле, полученном восстановлением прокаленного при 300 в течение 30 час. В первой работе [7] автор указывает, что, работая в пределах давления порядка 35 - 50 мм, он установил три вида адсорбции. Быстрая адсорбция, равновесие которой устанавливается практически сразу; медленная адсорбция, равновесие этой адсорбции устанавливаются в течение 15 - 20 час. Во второй работе Дзидзима [7] указывает, что если катализатор прокаливать при все повышающихся температурах, то второй вид адсорбции устраняется. [6]
Такие же выводы были сделаны при изучении адсорбции водорода, углекислого газа и этилена [16, 45, 46] на восстановленном никеле. Легко понять, что эти постоянные начальные дифференциальные теплоты адсорбции весьма трудно определить прямым калориметрическим методом, в особенности в системе вольфрам - водород. Следует отметить, что теплоты адсорбции, найденные прямым калориметрическим методом, не представляют собой истинные дифференциальные теплоты, а скорее являются интегральными теплотами адсорбции, полученными в определенном интервале покрытий поверхности. [7]
Этот метод оказался особенно полезным при изучении адсорбции водорода на никелевых и нанесенных катализаторах [3-8], для которых возможность определения форм сорбированного водорода электрохимическими методами ( потенциодинамическии метод, электропроводность, кривые заряжения) ограничена. [8]
Они нашли, что ото уравнение удовлетворительно описывает их опытные данные, полученные при изучении адсорбции водорода, кислорода и азота на угле из сахара при 78 и 195 К. [9]
Они нашли, что это уравнение удовлетворительно описывает их опытные данные, полученные при изучении адсорбции водорода, кислорода и азота на угле из сахара при 78 и 195 К. [10]
Рассмотрим на примере адсорбции водорода на платине и никеле, с какими осложнениями приходится сталкиваться при изучении адсорбции водорода на металлах. [11]
С позиционных представлений слабая адсорбция является следствием наличия ограниченного числа d - орбит, доступных для связывания. При изучении адсорбции водорода и этилена на различных переходных металлах Бик [31] отметил, что теплота хемо-сорбции уменьшается с уменьшением доступности атомных d - орбит. [12]
Выше мы видели, что на угле могут иметь место различные типы хемосорбции водорода. Эммет и Харкнесс [119] при изучении адсорбции водорода на железном катализаторе синтеза аммиака обнаружили два различных типа хемосорбции. Последние наблюдались в области соответственно - 100 и 100 С и были названы адсорбцией А - и 5-типа. Эти опыты были повторены Гаухмаиом и Ройтером [120], которые получили идентичные результаты. [13]
Таким образом, адсорбционный насос обладает относительно невысокой установившейся скоростью откачки углекислоты при давлениях ниже упругости пара ( из-за крайне замедленной диффузии газа в адсорбенте) и теоретически максимальной скоростью откачки ( конденсации) при давлениях выше упругости пара. Аналогичное явление очень медленного установления равновесия отмечено [50] при изучении адсорбции водорода на угле БАУ при 4 2 К. [14]
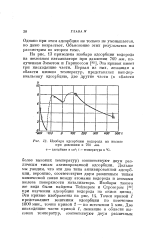 |
Изобара адсорбции водорода на железе при давлении в 760 мм. [15] |
Страницы: 1 2