Ориентированная адсорбция
Cтраница 3
На поверхности раздела металл - среда наряду с переносом зарядов проникают также процессы специфической адсорбции ионов и ориентированной адсорбции дипольных молекул. При этом поверхность металла обычно приобретает заряд одного знака, а прилегающий к металлу слой среды - равный по абсолютной величине заряд противоположного знака. Такую систему зарядов, подобную заряженному конденсатору определенной емкости Сдс ( е одной твердой и одной жидкой обкладкой), называют двойным слоем, а систему металл - электролит с двойным слоем на границе раздела фаз - электродом. [31]
 |
Схема определения энергии взаимодействия электрона с раствором.| Уровни энергии электрона в растворе. [32] |
Он возникает из-за изменения, при контакте с раствором, поверхностного скачка потенциала в металле, а также вследствие ориентированной адсорбции дипольных молекул растворителя на электроде. [33]
Ингибиторы коррозии действуют в топливе по одному из следующих механизмов: а) как поверхностно-активные соединения с образованием на металле защитной пленки вследствие ориентированной адсорбции полярных групп; б) оказывают нейтрализующее действие на кислые агрессивные продукты; в) химически взаимодействуют с металлом с образованием защитной пленки на его поверхности. [34]
При адсорбции ионов и создании двойного электрического слоя на поверхности коллоидных частиц гидрофиль-ность поверхности возрастает в результате собственной гидратации ионов и влияния зарядов поверхности на ориентированную адсорбцию дипольных молекул воды; так, например, возрастает смачивание заряженной поверхности ртути. Однако в этом случае гидратные слои полностью зависят от ионных взаимодействий и при наступлении коагуляции коллоидов электролитами не препятствуют процессам слипания частиц. Поэтому в типично лиофобных золях ( Au, Ag, S, AS2S3 и др.) сразу после перехода порога коагуляции наблюдается помутнение раствора, изменение цвета, выпадение осадка и другие проявления коагуляции. [35]
При адсорбции ионов и создании двойного электрического слоя на поверхности коллоидных частиц гидрофильность поверхности возрастает в результате собственной гидратации ионов и влияния зарядов поверхности на ориентированную адсорбцию дипольных молекул воды; так, например, возрастает смачивание заряженной поверхности ртути. Однако в этом случае гидратные слои полностью зависят от ионных взаимодействий и при наступлении коагуляции коллоидов электролитами не препятствуют процессу слипания частиц. Поэтому в типично лиофобных золях ( Аи, Ag, S, As2S3 и др.) сразу после перехода порога коагуляции наблюдается помутнение раствора, изменение цвета, выпадение осадка и другие проявления коагуляции. [36]
При адсорбции ионов и создании двойного электрического слоя на поверхности коллоидных частиц гидрофильность поверхности возрастает в результате собственной гидратации ионов и влияния зарядов поверхности на ориентированную адсорбцию дипольных молекул воды. Так, например, возрастает смачивание заряженной поверхности ртути. В этом случае гидратные слои полностью зависят от ионных взаимодействий и при наступлении коагуляции коллоидов электролитами не препятствуют процессам слипания частиц. Если же поверхность коллоидных частиц сама является гидрофильной или способна к образованию молекулярных соль-ватных слоев, коллоидные частицы могут сохраниться в состоянии золя даже при переходе порога коагуляции. Так, например, высокоочищенные золи кремнекислоты или А1203 могут сохраниться в растворе даже при падении электрофоретической подвижности ( - потенциала) почти до нуля. [37]
Можно указать два основных подхода к решению этой проблемы: в одних работах [3, 13-15] предполагается, что возникающие потенциалы в той или иной мере определяются ориентированной адсорбцией органических веществ, в других [1, 4, 5, 10, 12, 16] - адсорбированным водородом, появившимся на поверхности электрода в результате окисления исходных соединений. [38]
Поверхность твердого вещества всегда заряжена, хотя часто по совершенно разным причинам: благодаря тому, что она образована ионами, входящими в состав твердого вещества, вследствие ориентированной адсорбции дипольных молекул или ионов, или же, наоборот, вследствие ухода с нее ионов одного знака в окружающую среду ( раствор), или, наконец, в результате эмиссии или присоединения электронов под влиянием тех или иных условий, включая все виды воздействий, вызывающих появление статического электричества. Чистая поверхность слюды, например, заряжена положительно, так как она образована ионами К, а поверхность каолинита, построенная из ионов кислорода или гидро-ксила - отрицательно. Адсорбция противоположно заряженных ионов может нейтрализовать заряд поверхности или изменить его знак. При адсорбции кислорода на металлах образуется полярная связь М - О, причем кислородная поверхность приобретает отрицательный заряд, а примыкающий слой атомов металла - положительный. Адсорбция воды на металлах вызывает противоположный эффект: на поверхности образуется двойной электрический слой, обращенный к окружающей среде слоем не отрицательных, а положительных зарядов. [39]
На границе металл - раствор электролита могут протекать процессы перехода заряда из одной фазы в другую ( например, ионизация металла Me Me - f - e или разряд ионов металла Ме е Ме), специфическая адсорбция ионов электролита, ориентированная адсорбция полярных молекул. Поэтому в большинстве случаев поверхность металла приобретает электрический заряд одного знака, а прилегающий к металлу слой раствора - заряд противоположного знака. В наиболее простом случае, когда концентрация электролита в растворе достаточно высока ( - 1М), толщина заряженного слоя раствора становится наименьшей - примерно равной, радиусу гидратированного иона. [40]
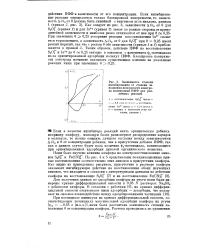 |
Зависимость степени ингибирования от степени заполнения поверхности электрода молекулами ПФФ для различных реакций. [41] |
Если в качестве ингибитора реакций взять органическую добавку, например камфору, имеющую более равномерное распределение зарядов в молекуле, то можно ожидать лучшего согласия между зависимостями A i / i0 и 0 от концентрации добавки, чем в присутствии добавок ПФФ, так как в данном случае будет мала величина - потенциала, возникающего при ориентированной адсорбции диполей органического вещества. [42]
Небольшие добавки ПАВ резко изменяют природу поверхностей и условия взаимодействия на границе битум - минеральный материал. Путем ориентированной адсорбции на поверхности с созданием мономолекулярного хемосорбционного слоя ПАВ способствуют образованию прочной связи между битумом и поверхностью минерального материала. Способность небольших количеств поверхностно-активных веществ изменять характер связи битума с поверхностью разных по природе минеральных материалов путем создания тонких адсорбционных слоев позволяет разработать новые технологические процессы приготовления асфальтобетона и других дорожных биту-моминеральных смесей. Особое значение при этом имеет модифицирование поверхности минеральных материалов с целью получения наибольшего структурообразующего влияния на тонкие пограничные слои битума, обеспечивающего повышение их прочности, водо-и теплоустойчивости и, следовательно, долговечности. [43]
Пенообразующая способность обусловлена ориентированной адсорбцией молекул поверхностно-активного вещества на границе его водного раствора и воздуха: за счет того, что воздух является неполярной средой, гидрофобные части молекул направлены в сторону воздуха, а гидрофильные - в сторону раствора. Такая ориентированная адсорбция приводит к снижению поверхностного натяжения, и при диспергировании воздуха в водном растворе моющего вещества образуется обильная пена. [44]
Вследствие ориентированной адсорбции перпендикулярно оси волокна они образуют вокруг волокна слой диэлектрика. Авторы выдвигают гипотезу, что ионогенные вещества обладают тем большим антистатическим действием, чем сильнее выражен их полярный характер или способность поляризоваться и чем длиннее углеводородная цепь их гидрофобной части. Закономерности для оксиэтилированных веществ, по-видимому, должны быть таким же. [45]
Страницы: 1 2 3 4