Изучение - выделение
Cтраница 2
Электрод, который предполагалось использовать для изучения выделения, составлял часть стенки электролизера и был достаточно топок для того чтобы сквозь него проходило излучение выделившегося на ном активного вещества. Излучение, свободно проходящее сквозь образованное электродом окошко, попадало в ионизационную камеру. Измеряемый ток насыщения пропорционален количеству выделившегося вещества. На рис. 1 показано расположение отдельных частей прибора. [16]
В работе [80 ] приведены реактивы для изучения выделений карбидов в нержавеющих сталях, содержащих, %: С 0 12; Сг 18 2; № 8 3 и С 0 16; Сг 21 4; Ni 21 3, после закалки с 950 - 1075 С и отпуска при 500 - 800 С. Изучена пригодность для электролитического травления растворов пикриновой и соляной кислот, хлорной кислоты и сульфата меди, хромового ангидрида и соляной кислоты, феррицианида калия и гидроксида калия. [17]
Первая серия опытов была проведена для изучения выделения углерода при различных соотношениях кислорода, содержащегося в катализаторе, и метана. Так как при температуре 950 С наблюдается спекание катализатора, исходной температурой для проведения первой серии опытов была принята температура 900 С. [18]
Большинство работ подобного рода относится к изучению выделения газов из минералов или искусственных поликристаллических образцов. В последнем случае выделение эманации ( Rn, Тп) используют для изучения, например, процессов рекристаллизации и спекания, изменения кристаллической модификации, реакций разложения и соединения в твердом состоянии и др. В основу эманационного периода положена химическая инертность благородных газов по отношению к веществу, в котором они находятся. [19]
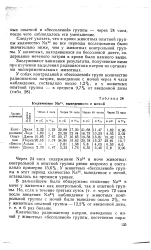 |
Количество Na24, выведенного с мочой. [20] |
Заслуживают внимания результаты, полученные нами при изучении выделения радиоизотопа натрия из организма экспериментальных животных. [21]
В другой работе [35] применено хроматографирование на бумаге для изучения выделения порфиринов с мочой кроликов, которым внутривенно вводили хлористый свинец. Выяснено, что преимущественно выделяется копропорфирин, что при стоянии вытяжки люминесценция усиливается и что лечение фолиевой кислотой не сказывается на выделении порфиринов. [22]
Британская исследовательская ассоциация по использованию угля, Лидархэд) указал, что Нэлиер в лаборатории Британской исследовательской ассоциации по использованию угля сделал некоторые расчеты, основанные на полученных им экспериментальных данных по изучению выделения летучих веществ из углей низкой степени углефикащии, определил значения энергии активации в области температур 320 - 480, которые составили 40 5 ккал / моль и были одинаковы для грех проб. Это подтверждает, что основной процесс, протекающий в этих углях, один и тот же, хотя, летучие продукты разложения при 360 - 420 могут несколько отличаться в результате воздействия выделяющихся соединений, содержащих кислород. [23]
Ультрамикроэлектродами называют электроды с необычайно малыми размерами - от нескольких нанометров до 20 - 50 мкм. Идея создания таких электродов возникла в результате изучения выделения зародышей капелек ртути при электролизе ее солей на угольном электроде. Впоследствии для изготовления УМЭ стали применять тонкие Pt -, Ir -, Аи - или Ag-проволоки, впаянные в стекло, а также углеродные волокна диаметром от 0 3 до 20 мкм. Металлические УМЭ обычно изготавливают из литого микропровода, который истончают электролитически до нужной толщины после впаивания в стеклянный капилляр. Электроды из углеродных волокон помещают в полимерные матрицы. Композиционные УМЭ изготавливают путем диспергирования графитового порошка в связующем с последующим спеканием при температуре около 1000 С. Такие электроды состоят из большого числа проводящих микроучастков, разделенных на изолированные сегменты сопоставимых размеров. Ртутные УМЭ получают путем электролитического выделения капелек ртути на поверхности иридиевого или углеродного дискового УМЭ. [24]
Позднее Кошем и Гайсинским [20 41] было изучено более детально влияние природы электрода на критический потенциал полония. В случае полония это изучение могло быть распространено лишь на небольшое число металлов. Нормальный потенциал полония лежит, по-видимому, вблизи нормального потенциала серебра; из этого следует, что кроме платины, золота и серебра, немногие металлы имеют в кислом растворе спонтанные потенциалы, настолько положительные, чтобы быть поляризованными достаточно отрицательно, а изучение выделения полония на других металлах требует особых приемов. [25]
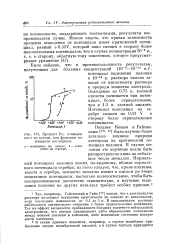 |
Процент Ро, осажденного на катоде, как функция потенциала последнего. [26] |
Позднее Кошем и Гайсин-ским [20 41] было изучено более детально влияние природы электрода на критический потенциал полония. В случае полония это изучение могло быть распространено лишь на небольшое число металлов. Нормальный потенциал полония лежит, по-видимому, вблизи нормального потенциала серебра; из этого следует, что, кроме платины, золота и серебра, немногие металлы имеют в кислом растворе спонтанные потенциалы, настолько положительные, чтобы быть поляризованными достаточно отрицательно, а изучение выделения полония на других металлах требует особых приемов. [27]
Отлагается во всех органах и тканях, в том числе в коже, вояосах, шерсти. В хронических опытах Sb отлагается в органах в больших количествах, чем при острых отравлениях. Выделение происходит медленно, в основном с мочей, в незначительных размерах с калом. Изучение выделения радиоактивной Sb показало, что у человека в 50 % случаев выделение введенной дозы рвотного камня происходит только за 500 час. [28]
Азот в атомарной форме растворяется в а-железе и может диффундировать через него. При этом количество поглощенного азота достигает 0 4 атомн. Железо дает с азотом несколько различных соединений переменного состава. Известен, например, е-нитрид железа, в котором атомы железа образуют плотно упакованную гексагональную решетку, а атомы азота упорядоченно располагаются в междуузлиях октаэдров. Нитрид при 400 С может содержать от 35 3 до 49 3 атомов азота на 100 атомов железа. Атомы азота легко диффундируют через такую решетку. Гудив и Джэк [172] при изучении выделения газообразного азота из этого твердого раствора установили, что атомы азота при выходе на поверхность ведут себя, как частицы двумерного газа, и соединяются с образованием молекул азота, которые десорбируются с поверхности. Скорость данного процесса определяется скоростью образования молекул азота из двух хемосорбированных атомов. [29]
Азот в атомарной форме растворяется в а-железе и может диффундировать через него. При этом количество поглощенного азота достигает 0 4 атомн. Известен, например, е-нитрид железа, в котором атомы железа образуют плотно упакованную гексагональную решетку, а атомы азота упорядоченно располагаются в междуузлиях октаэдров. Нитрид при 400 С может содержать от 35 3 до 49 3 атомов азота на 100 атомов железа. Атомы азота легко диффундируют через такую решетку. Гудив и Джэк [172] при изучении выделения газообразного азота из этого твердого раствора установили, что атомы азота при выходе на поверхность ведут себя, как частицы двумерного газа, и соединяются с образованием молекул азота, которые десорбируются с поверхности. Скорость данного процесса определяется скоростью образования молекул азота из двух хемосорбированных атомов. [30]
Страницы: 1 2 3