Изоэлектрическое фокусирование
Cтраница 1
Изоэлектрическое фокусирование в геле имеет определенные преимущества по сравнению с ИФ в среде со стабилизованным градиентом плотности. Эти преимущества состоят в следующем: 1) сокращается длительность разделения; 2) полностью подавляется термическая конвекция; 3) применяется простое оборудование для ИФ; 4) возможно одновременное разделение нескольких образцов; 5) возможно обнаружение с помощью различных красителей и различных методик; 6) возможно объединение ИФ и зонного электрофореза в двухмерном варианте; 7) достаточно небольшого количества образца; 8) возможно обнаружение белков методом иммунодиффузии. Однако при применении геля возникают проблемы, связанные с молекулярно-ситовым эффектом, который имеет место в основном при разделении больших молекул. [1]
Изоэлектрическое фокусирование является важным дополнением к другим методам разделения белков; многочисленные ссылки, касающиеся этого метода, приведены в гл. Ригетти и Драйсдейл [204] в общем обзоре по изоэлектриче-скому фокусированию в гелях также приводят примеры работ с тонкими слоями, особенно при двумерном разделении. [2]
Изоэлектрическое фокусирование в тонких слоях имеет ряд преимуществ перед другими вариантами этой методики [211]: обеспечивает легкость нанесения образца, позволяет применять простые приборы, экономит дорогие амфолитные носители, позволяет разделять в одинаковых условиях одновременно несколько смесей, причем высокая разделительная способность при этом сохраняется. [3]
Изоэлектрическое фокусирование включает электрофоретическую миграцию белка в условиях градиента рН, которая продолжается до тех пор, пока белок не достигнет такой области, где рН равен р / белка. Суммарный заряд белка становится равным нулю, и белок концентрируется в этой области в виде узкой зоны. Любое перемещение белка из-за диффузии в сторону от этой зоны ведет к восстановлению его электрического заряда и, следовательно, к электрофоретической миграции в обратном направлении. Итак, при изоэлектрическом фокусировании электрофорети-ческий массоперенос и зональная диффузия совместно обусловливают стационарность процесса. [4]
Изоэлектрическое фокусирование [42 - 45] в линейном градиенте рН позволяет разделить белки, характеризующиеся различными изоэлектрическими точками. При движении в градиенте рН суммарный заряд белка постоянно меняется, и в области рН, близких к изоэлектрической точке, становится равным нулю. Соответствующий белок фокусируется, образуя узкую зону. При препаративном фокусировании в колонке стабилизация градиента рН осуществляется с помощью градиента плотности используемого буферного раствора, однако чаще работают с плоскими слоями полиакриламидного или гранулированного геля. При разделении сыворотки образуется более 40 белковых полос. [5]
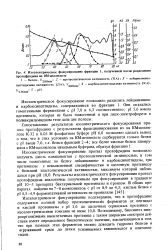 |
Изоэлектрическое фокусирование фракции 1, полученной после разделения протофрадина на КМ-целлюлозе. [6] |
Результаты изоэлектрического фокусирования протеаз протофрадина аналогичны полученным при фокусировании в градиенте рН 10 - 3 препарата бактериальной протеиназы и проназы. [7]
Электрофокусирование ( изоэлектрическое фокусирование) проводят в градиенте рН, который формируется при пропускании электрического тока через стабилизованный буфер, содержащий смесь амфоли-тов. [8]
Хотя в настоящее время существуют методы определения изоэлектрической точки исследуемых белков с достаточной точностью ( например, изоэлектрическое фокусирование в градиенте плотности сахарозы), знание изоточки вовсе не обязательно для выбора ионообменника. Пригодность того или иного ионита легко определить по степени связывания белка в статических условиях. В случае анионита смолу приводят в равновесие с буферным раствором, рН которого соответствует верхней границе области устойчивости исследуемого белка. [9]
Мало того, в ходе элюции будет происходить сужение белковых зон, подобно тому как это происходит при изоэлектрическом фокусировании. Действительно, белки из передней части зоны конечной ширины раньше всего окажутся в области щелочных рН, диктующих замедление их движения и сорбцию на новом участке колонки. [10]
Резюмируя материал по традиционным способам очистки цел-люлаз, следует отметить, что набор данных методов позволяет за 3 - 5 стадий получить гомогенные по данным изоэлектрического фокусирования и электрофореза компоненты целлюлазного комплекса. Эта задача решается сравнительно легко, если требуется выделить и очистить одну или несколько основных множественных форм. Однако она становится часто неразрешимой при получении в высокоочищенном состоянии всех множественых форм целлюлаз, полного фракционирования комплекса как в силу высокой трудоемкости ( несколько месяцев), так и за счет принципиальной невозможности разделения некоторых близких по всем биохимическим параметрам множественных форм, крайне низких ( 5 - 10 %) выходов ферментов. [11]
Резюмируя материал по традиционным способам очистки целлюлаз, следует отметить, что набор данных методов позволяет за 3 - 5 стадий получить гомогенные по данным изоэлектрического фокусирования и электрофореза компоненты целлюлазного комплекса. Эта задача решается сравнительно легко, если требуется выделить и очистить одну или несколько основных множественных форм. Однако она становится часто неразрешимой при получении в высокоочищенном состоянии всех множественых форм целлюлаз, полного фракционирования комплекса как в силу высокой трудоемкости ( несколько месяцев), так и за счет принципиальной невозможности разделения некоторых близких по всем биохимическим параметрам множественных форм, крайне низких ( 5 - 10 %) выходов ферментов. [12]
Только при электрофорезе с подвижной границей и при зонном электрофорезе наблюдается постоянство рН во всей среде и постоянно расходящееся движение компонентов исследуемой смеси. Изоэлектрическое фокусирование может приводить к максимальным величинам рН при нулевой результирующей подвижности разделяемых компонентов. [13]
Наиболее часто применяемым способом выделения щелочных протеиназ является фракционирование проназы на КМ-целлюлозе с последующей очисткой фракций, содержащих трипсино - и химотрипсинопо-добиые ферменты, на различных ионообменниках и сефадексах. Гомо - leiiHocib полученных щелочных протеиназ в большинстве случаев подтверждают результатами седиментационного анализа, электрофорезом в полиакриламидном геле, методом изоэлектрического фокусирования, эквимолярным включением 32 Р ДПФФ. [14]
Определение модифицированного остатка внутри биополимера с известной первичной структурой является конечной и наиболее трудоемкой стадией эксперимента. Обычным способом определения ( локализации), модифицированного остатка в белке является первоначально ферментативное или химическое расщепление биополимера на небольшие пептидные фрагменты, разделение их методом электрофореза, изоэлектрическим фокусированием или хроматографически и идентификация модифицированного пептида. Идентификацию провести достаточно легко, так как модифицированный пептид смещается относительно немоди-фицированного в стандартной системе разделения. Далее может быть проведена процедура ступенчатой деградации по Эдману до тех пор, пока на одной из ступеней не образуется фенилтиогидантоиновое производное с характеристикой, например хроматографической подвижностью, не свойственной фенилтиогидан-тоинам известных аминокислотных производных. [15]
Страницы: 1 2