Форма - кресло
Cтраница 4
 |
Ньюменовская проекция циклогексана. [46] |
Эти факторы определяют большую стабильность формы кресла по сравнению с другими конформерами циклогексана. [47]
 |
Инверсия формы кресла. [48] |
В процессе отгибания верхней части формы кресла ( flipping), или инверсии формы кресла, все экваториальные связи становятся аксиальными и все аксиальные связи превращаются в экваториальные. Инверсия формы кресла осуществляется легко. Это следует из того, что в спектрах ядерного магнитного резонанса протоны циклогексана имеют один четкий сигнал. Поскольку аксиальные и экваториальные протоны циклогексана дают сигналы в различном поле [26] ( см. также разд. [49]
Хронологически первое подтверждение большей устойчивости формы кресла для циклогексана было дано рентгенографическими исследованиями. [50]
 |
Структурные данные для тра с-дихлоро-1 4 8 11-тетра-азациклотетрадеканникеля ( П. [51] |
Шестичленные кольца находятся в кон-формациях формы кресла. [52]
Молекулы стероидов имеют чаще всего форму кресла и изогнуты так, что циклогексановые кольца лежат в различных плоскостях; изменения конформации, введение заместителей или двойных связей в каркас стероидной молекулы сильно сказывается на ее биологической активности. [53]
Карбонильная группа циклогексанона, имеющего форму кресла ( I), является внутренне симметричным хромофором. В другом варианте молекулы ( III), имеющей форму кресла, единственный асимметричный заместитель - метильная группа - расположен уже в отрицательном октанте, и можно предсказать, что эффект Коттона будет отрицательным. Наконец, в скрученной форме ( IV) само кольцо циклогексанона становится асимметричным. [54]
Переход от структуры Хеуорса к форме кресла пиранозы начинают с атома кислорода гетероцикла, который находится в верхнем правом углу шестиугольной проекции Хеуорса, в то время как полуацетальный углеродный атом ( С1) занимает крайнее правое положение. Затем рисуют соответствующую форму кресла с гетероциклическим атомом кислорода в верхней правой точке. [55]
Это объяснялось конформационным равновесием между формой кресла ( XVa) ( полярный растворитель) с аксиальной гидроксильной группой, неспособной к образованию внутримолекулярной водородной связи, и конформацией ванны ( XV6) х, в которой возможна водородная связь между экваториальной гидроксильной и карбоксильной группами. Эти выводы согласуются как с предсказаниями, полученными из правила октантов ( положительный эффект Коттона для XVa и отрицательный - для XV6) T3K и с наблюдаемыми [83] сдвигами по длинам волн. [56]
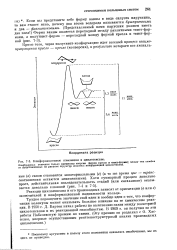 |
Конформащюшше изменения в циклогексане. [57] |
Конформерам отвечают только минимумы энергии ( форма кресла и твист-форма); между тем каждая из представленных на рисунке структур является конформацией циклогексана. [58]
В i а шобра июм состоянии форма кресла частично переходит в форму ванны, энергия которой приблизительно на Г) 6 ка. [59]
Страницы: 1 2 3 4