Форма - орбиталь
Cтраница 3
 |
Форма молекулярной ст-орбита-ли для полярной молекулы LiH. [31] |
Ковалентная полярная связь возникает между атомами разных элементов. Так как в этом случае электроны на орбиталях атомов обладают различной энергией, при образовании связи искажаются граничные поверхности молекулярных орбиталей, и вероятности пребывания электрона в разных частях пространства также будут разные, поскольку форма орбиталей сделается асимметричной относительно ядер атомов. [32]
 |
Изображение 2рг - орбитали. [33] |
Если требуется показать на рисунке точное значение волновой функции, то пользуются контурными диаграммами, где линии соединяют точки, для которых г ( или if2) имеет определенное значение. На рис. 1.8 показаны различные изображения 2р2 - орбитали атома водорода. Форма орбиталей важна для понимания особенностей химической связи, и в дальнейшем мы неоднократно будем пользоваться подобными изображениями орбиталей. На схемах часто рисуют орбитали стилизованно, несколько искажая их форму и пропорции. [34]
При переходе от атома водорода к атомам других элементов условимся, что формы s -, р -, d - и / - орбиталей, изображенные схематически на рис. 18.1 - 18.3, качественно остаются теми же. Поэтому при описании формы орбиталей атомов различных элементов считают их примерно такими же, как и в возбужденном атоме водорода. [35]
Наиболее часто употребляемое приближение состоит в том, что многоэлектронные волновые функции записывают в виде произведений одноэлектронных волновых функций, аналогичных тем, которые получаются при решении задачи для атома водорода. Эти одноэлектрон-ные функции, используемые для построения многоэлектронной волновой функции, называют атомными орбиталями. Их также называют водородоподобными орбиталями, поскольку они являются одно-электронными орбиталями и их форма аналогична форме орбиталей самого атома водорода. Коулсон [10] называл атомные орбитали персональными волновыми функциями, желая этим подчеркнуть, что в данной модели каждый электрон занимает индивидуальную орбиталь. [36]
Для орбиталей с / 0 имеется ( 2 / 1) способа, которыми орбиталь данной формы может быть ориентирована в пространстве. Наложение магнитного поля снимает вырождение орбиталей одинаковой формы. В этом случае значения углового момента будут различными вдоль разных осей, что соответствует разной ориентации одинаковых по форме орбиталей в пространстве. Конечно, в многоэлектронных атомах с большим числом заполненных орбиталей можно ожидать мгновенного появления выступов электронного облака, но общее распределение электронной плотности сферически симметрично. [37]
Объяснить закономерности, выраженные рядом Ирвинга - Вильямса, можно с позиций теории кристаллического поля. Эта электростатическая теория не принимает во внимание особенности строения электронных оболочек лигандов, а рассматривает последние как точечные отрицательные заряды, располагающиеся в определенной геометрической конфигурации вокруг центрального катиона с положительным зарядом. В отличие от упрощенной электростатической теории, рассматривающей взаимодействие между точечными частицами она учитывает энергетические изменения в системе, связанные с формой орбиталей d - электронов. [38]
 |
Слева-орбитали парныхфункиий ( У и валентных молекулярных орбиталей ( 2. справа - орбитали, полученные при полном отказе от условий ортогональности для. [39] |
Орбитали остовной парной функции оказываются практически идентичными. У парной функции валентных орбита-лей, как и у молекулярной орбитали, обнаруживается узел. Однако он обнаруживается в области, где электронная плотность определяется главным образом остовной орбиталью, и ограничения на ортогональность (2.6.16) незначительно влияют на форму орбиталей в химически важной валентной области. [40]
Классификация С-С - связевых орбиталей в этилене как двух а - и двух я-спин-орбиталей - до сих пор наиболее удобная и единственная нужная нам в дальнейшем классификация. Рассмотрим одно из таких представлений отчасти потому, что оно вводит новый тип преобразований, частью потому, что оно иллюстрирует опасность приписывания слишком большого значения форме индивидуальных орбиталей в многоэлектронной волновой функции и, наконец, из-за того, что оно дает интересную связь с доквантово-механическим описанием кратных связей в виде изогнутых связей. [41]
Классификация С-С - связевых орбиталей в этилене как двух а - и двух л-спин-орбиталей - до сих пор наиболее удобная и единственная нужная нам в дальнейшем классификация. Рассмотрим одно из таких представлений отчасти потому, что оно вводит новый тип преобразований, частью потому, что оно иллюстрирует опасность приписывания слишком большого значения форме индивидуальных орбиталей в многоэлектронной волновой функции и, наконец, из-за того, что оно дает интересную связь с доквантово-ыеханическим описанием кратных связей в виде изогнутых связей. [42]
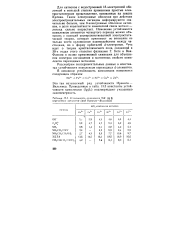 |
Устойчиаость комплексов MR ( Ig f ( переходных элементов ( ряд Ирвинга-Вильямса. [43] |
Для катионов с недостроенной 18-электронной оболочкой в меньшей степени применимы простые электростатические представления, основанные на законе Кулона. Такие электронные оболочки при действии электроотрицательных лигандов деформируются значительно больше; чем 8-электронные оболочки катионов, и доля ковалентности химической связи металл - лиганд сильно возрастает. Изменение устойчивости комплексов элементов четвертого периода можно объяснить с позиций усовершенствованной электростатической теории, которая принимает во внимание не только чисто кулоновское взаимодействие между частицами, но и форму орбиталей d - электронов. [44]
В уравнениях ( 2) и ( 3) отсутствуют значения sin ц cos углов 6 и ср. Это может быть только при сферической форме орбиталей. В уравнениях ( 4), ( 5) и ( 6) имеются значения sin и cos, 9 и ф, и это приводит к заключениям о несферической форме орбиталей, и что они ориентированы по направлению трех осей координат. [45]
Страницы: 1 2 3 4