Молекулярная форма
Cтраница 2
Помимо молекулярной формы химических уравнений пользуются иной формой, более соответствующей действительно происходящей в водных растворах реакции. [16]
В молекулярной форме в топливе находятся газы, иод, цезий, теллур, рутений. Лантан, цезий и цирконий образуют растворимые оксиды, возможно образование метилиодида и йодистого цезия. Можно полагать, что из перегретого и оплавленного топлива иод выходит в молекулярной форме, остальные нуклиды - в молекулярной и аэрозольной форме. В начальный период аварии значительная часть молекул и паров летучих нуклидов становится аэрозолями за счет улавливания мелкодисперсной капельной влагой, а затем - твердыми аэрозолями, образующимися при конденсации перегретых материалов активной зоны. [17]
В молекулярной форме это уравнение имеет вид: К. [18]
В молекулярной форме существует более 7 миллионов описанных веществ при практической неограниченности числа комбинаций различных атомов в форме молекул. [19]
Объем двух молекулярных форм Ас и А / можно считать одинаковым, на-площади поверхности, способной образовывать внешние контакты, у этих форм Разные. На поверхности формы Ас отсутствует контактный участок Н, уменьшена площадь контактного участка эфирного кислорода. [20]
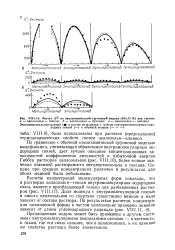 |
Расчет GE по квазихимической групповой модели ( 308 15 К для систем. [21] |
Расчеты концентраций молекулярных форм показали, что в растворах целлозольв-гексан внутримолекулярная водородная связь является преобладающей только для разбавленных растворов ( рис. VIII. Доля молекул с внутримолекулярной связью в смесях целлозольвов со спиртами существенно меньше и мало зависит от состава раствора. [22]
Учет этих молекулярных форм в паре позволяет получить соотношения, описывающие изотермы давления насыщенного пара для совершенных ионных и регулярных жидких растворов, применительно в рассматриваемым системам. К ( С1Вг), K ( Cll), K ( Brl) t ( К Na) Brn K ( ci Br - l), в пределах ошибки опыта совпадают с теоретически рассчитанными что является веским доводом в пользу рассматриваемых моделей пара и и расплава. [23]
Максимумы светопоглощения молекулярных форм нафтольных; производных находятся при 470 - 500 нм. Все реагенты, растворен - ные в органических растворителях и водноорганических смесях, имеют близкие по цвету окраски - от желтых до оранжевых. При V / подкислении наблюдается гипсохромный сдвиг максимумов светопоглощения и уменьшение интенсивности поглощения. [24]
Спектры поглощения молекулярной формы реагента ( рН 1 - 2) и анионной формы ( рН 13) показаны на рисунке. [25]
Константы распределения молекулярной формы оксихинолина ( Рид) равны: 122 - для бензола, 353-для хлороформа, 140 - для метилизобутилкетона. [26]
Константы распределения молекулярной формы оксихинолина ( РИА) равны: 122 - для бензола, 353-для хлороформа, 140 - для метилизобутилкетона. [27]
Максимумы светопоглощения молекулярных форм нафтольных производных находятся при 470 - 500 нм. Все реагенты, растворенные в органических растворителях и водноорганических смесях, имеют близкие по цвету окраски - от желтых до оранжевых. При подкислении наблюдается гипсохромный сдвиг максимумов светопоглощения и уменьшение интенсивности поглощения. Это объясняют тем, что протон, связывая электронную пару гетероциклического атома азота, выключает ее из цепи сопряжения, уменьшая подвижность электронного облака и увеличивая энергию электронов в цепи сопряжения. [28]
Водород в молекулярной форме не способен проникать в металл катода, он удаляется с его поверхности, диффундируя в раствор электролита и в виде газовых пузырьков. На некоторых металлах, например на никеле, пузырьки водорода, в отсутствии специально введенных смачивающих катод добавок ПАВ, удерживаются на поверхности металла и могут застраиваться в кристаллизующийся электроосадок, что ведет к питтингообразованию. [29]
 |
Измерение повышения температуры кипения ( по Ландсбер-геру. [30] |
Страницы: 1 2 3 4