Молекулярная форма
Cтраница 3
В какой молекулярной форме присутствует сера, растворенная в CS2, если раствор, содержащий 3 82 г серы в 100 0 г CS2, кипит при 46 48 С. [31]
Водород в молекулярной форме никаких спектральных линий в радиодиапазоне не излучает. Сведения о плотных облаках МЗС, где основную массу составляют молекулы Н2, большей частью были получены по вращательным линиям других молекул, находящихся в этих облаках. Частоты этих линий приходятся в основном на миллиметровые и сантиметровые волны. [32]
Молекула с другой молекулярной формой может реагировать по-иному. [33]
 |
Периодичность в изменении температур плавления гомоатомных соединений.| Энергии диссоциации двухатомных молекул гомоатомных сое. [34] |
Таким образом, молекулярная форма в парообразном состоянии характерна для неметаллов. Большинство же металлов ( за исключением щелочных и меди) при высоких температурах существует в виде одноатомного пара. [35]
Такого рода изменчивость молекулярных форм, неизбежно связанную с конденсированным состоянием вещества, следует рассматривать как естественный способ компенсации, отражения воздействия молекул друг на друга, так как логично предположить, что вся материя обладает свойством, по существу родственным с ощущением, свойством отражения. [36]
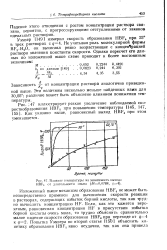 |
Влияние температуры на зависимость выхода HBF4 от длительности опыта ( М0 0788, 04. [37] |
Не учитывая роль молекулярной формы BF3 - H2O, он вычислил резко возрастающие с концентрацией раствора значения константы скорости. [38]
Какая из двух развернутых молекулярных форм 1 [ ( NH3) sCo - CN - - Co ( CN) 5 ] или [ ( МНзЬСо-NC-Co ( CN) 5 ] более вероятна и почему. [39]
Сравнительно высокая прочность молекулярных форм кислорода является основой рассматриваемой ниже перекисной теории, которая утверждает существование большого класса перекисных соединений, наряду с соединениями, содежащими атомарные формы кислорода. [40]
Можно полагать, что молекулярная форма HBF4 не существует и в растворе. [41]
И сейчас еще изменчивость молекулярных форм рассматривается как свойство изолированных молекул, а не как продукт взаимодействия внутри - и межмолекулярных сил. Возможностью структурных изменений, неизбежно связанных с агрегацией молекул ( и в чистых фазах и в растворах), как правило, пренебрегают. В жидком же состоянии становятся возможными и некоторые формы поворотных изомеров, обычно отсутствующие как нестабильные, в парах и превращающиеся в транс-состояние. [42]
Такого жо рода изменчивость молекулярных форм, включая и способ агрегации молекул в первичные структурные группы - ассоциации ближнего порядка, является также источником разнообразия реакционной активности одного и того же вещества в различных средах. Она же лежит и в основе такого интересного явления в стереохимии, как полиморфизм. [43]
Неорганическая химия рассматривает множество геометрических молекулярных форм даже для соединений одного элемента. Поэтому неорганическая химия была и в большей степени остается областью химии, в которой основное внимание уделяется строению реагентов и продуктов, без исследования путей превращения первых во вторые. Причина тому - малое число однозначных данных по механизмам реакций. Однако в последнее время ситуация меняется. Внимание исследователей все более концентрируется на том, как неорганическая молекула изменяется и реагирует. Большинство таких исследований проведено с использованием комплексных соединений и обсуждается в разд. [44]
Для получения той или иной конкретной молекулярной формы серы используют фотолиз ее соединений или подходящие и химические превращения. [45]
Страницы: 1 2 3 4