Окисленная форма - индикатор
Cтраница 1
Окисленная форма индикатора Indox при этом должна иметь иной цвет, чем восстановленная форма Indued. [1]
Окисленная форма индикатора красного цвета, восстановленная - бесцветная при нормальном окислительном потенциале ниже 1 08 В. В присутствии Н2Сг2О7 индикатор окисляется и раствор окрашивается в красный цвет. [2]
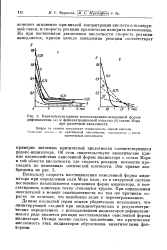 |
Кинетические кривые восстановления окисленной формы. [3] |
Поскольку скорость восстановления окисленной формы индикатора при определении соли Мора мала, то в титруемой системе постепенно накапливается окрашенная форма индикатора, и констатировать конечную точку становится трудно. При определении окислителей в момент эквивалентности по тем же причинам окраска не исчезает, что неизбежно ведет к перетитровыванию. [4]
Вблизи конечной точки титрования окисленная форма индикатора восстанавливается с трудом. При титровании в сернокислой среде переход окраски нитроферроина происходит при слишком высоком значении потенциала; окраска ферроина исчезает очень медленно, поэтому предпочтительнее пользоваться ферроином, чем проводить титрование без индикатора, используя окраску ионов самого Ceiv. Баер и Штейн [72] показали, что при использовании очень чистого CeIV стехиометрические соотношения выполняются точно. При титровании же церием обычной реактивной квалификации при избытке пероксида водорода возможна погрешность в результате каталитического разложения пероксида водорода; однако если в избытке находится церий ( IV), то результаты всегда оказываются очень точными. [5]
Показано, что реакция восстановления окисленной формы изученных индикаторов при высоких значениях кислотности по скорости является лимитирующей стадией процесса титрования. [6]
Показано, что реакция восстановления окисленной формы изученных индикаторов в сильнокислых растворах по скорости является лимитирующей стадией процесса титрования. [7]
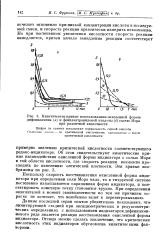 |
Кинетические кривые восстановления окисленной формы. [8] |
Об этом свидетельствуют кинетические кривые взаимодействия окисленной формы индикатора с солью Мора в той области кислотности, где скорость реакции возможно проследить по изменению оптической плотности. [9]
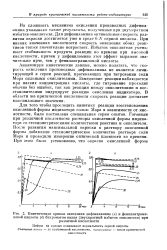 |
Кинетические кривые окисления дифениламина ( а и фенилантраниловой кислоты ( б бпхроматом калия ( двухкратный избыток окислителя при. [10] |
Для того чтобы проследить кинетику реакции восстановления окисленной формы индикатора солью Мора в зависимости от кислотности, была поставлена специальная серия опытов. [11]
Эта полуреакция подразумевает, что в преобразовании окисленной формы индикатора в восстановленную не участвуют ионы водорода. Хотя такое утверждение и справедливо для некоторых редокс индикаторов, в действительности же ионы водорода участвуют в окислительно-восстановительных реакциях большинства индикаторов. [12]
Если дать раствору постоять, то он постепенно снова приобретает окраску окисленной формы индикатора и затем можно отметить четкую конечную точку. Ричардсон и Брайсон43 указывают, что в момент, совпадающий с появлением ложной конечной точки, наблюдается падение потенциала, а затем снова происходит подъем потенциала, соответствующий возобновлению прежней окраски индикатора. Появление ложной конечной точки объясняется, по-видимому, адсорбцией ионов цинка на поверхности осадка до наступления конечной точки. После перехода изоэлектрической точки осадок коагулирует, при этом освобождаются ионы цинка, которые реагируют с ионами гексацианоферрата ( II), временно оказавшимися в избытке. [13]
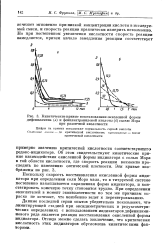 |
Кинетические кривые восстановления окисленной формы. [14] |
Данные последней серии опытов убедительно показывают, что-лимитирующей стадией при оксидиметрических и редуктометри-ческих определениях с использованием индикаторов дифенилами-нового ряда является реакция восстановления окисленной формы индикатора. Отсюда можно сделать заключение, что критическая кислотность этих индикаторов обусловлена кинетическими факторами. [15]
Страницы: 1 2