Окисленная форма - индикатор
Cтраница 2
Если концентрация закисного железа в пробе будет ниже заданной, реакция окисления успеет пройти и цвет раствора в пробе станет темно-пурпурным, что соответствует окисленной форме индикатора. Вследствие наличия в устройстве сравнительного светофильтра 19 со спектральной характеристикой и оптической плотностью, соответствующей спектральной характеристике и плотности раствора в момент подхода последнего к эквивалентной точке титрования, выходящий из датчика электрический сигнал переменного тока, снимаемый с фотосопротивления 22, меняет амплитуду и фазу в зависимости от преобладания в рабочей кювете 17 титровальной ячейки 16 датчика окисленной или восстановленной формы индикатора или, что то же самое, в зависимости от концентрации закисного железа в титровальной ячейке ( больше или меньше заданной) и направляется на блок непрерывной отработки эквивалентной точки титрования 6, где усиливается и преобразуется. Последний управляет с помощью исполнительного механизма 8 и регулирующего клапана 9 подачей окислителя ( МпО2) в реактор из бака, тем самым поддерживая концентрацию закисного железа в реакторе на заданном уровне. [16]
При использовании в качестве восстановителя As111, а в качестве окислителя CeIV в серной кислоте наблюдается прямо противоположная картина. Окисленная форма индикатора, ферроин, почти не восстанавливается избытком As 1 даже в присутствии катализатора - четырехокиси осмия. В то же время добавление лишь одной капли раствора CeIV быстро вызывает появление красной окраски ( ферроина) - совершенно очевидно, в результате индуцированной реакции. [17]
Вблизи конечной точки окисленная форма индикатора восстанавливается с трудом. При титровании в сернокислой среде переход окраски нитроферроина происходит при слишком высокой величине потенциала; окраска ферроина исчезает очень медленно, поэтому вместо того чтобы проводить титрование без индикатора, используя окраску ионов самого CeIV, все же предпочтительнее пользоваться ферроином. Баер и Штейн 50 показали, что при употреблении очень чистого CeIV стехиометрические соотношения точно выполняются. При титровании же церием обычной реактивной квалификации в случае избытка перекиси водорода имеет место ошибка в результате каталитического разложения перекиси водорода; однако если в избытке находится церий ( IV), то результаты всегда оказываются очень точными. [18]
При титровании двухвалентного железа бихроматом калия небольшие количества ванадия не влияют на определение железа, так как четырехвалентный ванадий не окисляется бихроматом калия. Однако в присутствии больших количеств ванадия влияние восстановительного потенциала четырехвалентного ванадия возрастает настолько, что происходит обесцвечивание синей окисленной формы индикатора дифениламина или дифениламинсульфо-ната натрия. Вследствие этого конечная точка титрования получается неотчетливой, а это обычно приводит к тому, что раствор оказывается перетитрованным и результат определения железа получается несколько завышенным. В таких случаях во избежание влияния ванадия в раствор рекомендуется добавлять - 3 г NH4F, который связывает V ( IV) и Fe ( III) в комплексные соединения, не действующие на индикатор. [19]
Эти индикаторы - преимущественно окрашенные органические соединения, которые изменяют свой цвет в зависимости от окислительно-восстановительного потенциала титруемой системы. При введении избытка окислителя образуется окисленная форма индикатора, а прибавление избытка восстановителя приводит к образованию его восстановленной формы. Процесс перехода окисленной формы в восстановленную и обратно, сопровождающийся изменением окраски, можно повторить много раз без разрушения индикатора. [20]
Ферроин имеется в продаже и теперь широко применяется при титровании сильными окислителями, например: солями церия ( IV), бихроматом и перман-ганатом. Изменение окраски очень четкое и обратимое. Избыток окислителя очень медленно влияет на окисленную форму индикатора, хотя в кислых растворах при высоких температурах его действие значительно ускоряется. Индикаторные поправки и различные методы анализа, в которых этот индикатор применялся, будут рассмотрены нами в III томе. [21]
Бихромат калия окисляет дифениламин, и смесь приобретает красно-бурую окраску. При титровании солью Мора шестивалентный хром восстанавливается в трехвалентный, в результате цвет раствора постепенно переходит в синий, а к концу титрования в сине-фиолетовый. Когда же весь хром будет оттитрован, последующее добавление соли Мора вызывает переход окисленной формы индикатора в восстановленную ( бесцветную); появляется зеленая окраска, которую придают раствору ионы трехвалентного хрома. Четкому переходу сине-фиолетовой окраски в зеленую мешают ионы трехвалентного железа, появляющиеся в процессе реакции. Чтобы сделать более ясным конец реакции, титрование проводят в присутствии ортофосфорной кислоты, которая связывает ионы Fe3 в бесцветный комплексный ион [ Fe ( PO4) 2 ] 3 - и предохраняет дифениламин от окисления. [22]
Последние - это красители, образующие со своими лейкоформами обра - Щ - - 5 4 тимые окислительно-восстановительные системы, свойства которых будут рассмотрены в гл. IV - III.5. Съе-Применение окислительно-восстановительных ин - ная кювета для дикаторов основано на том, что при достижении спектрофотометри-равновесия окислительные потенциалы исследуе - растворов мой и индикаторной систем становятся равными. Потенциал индикаторной системы легко опреде - i - шлиф а - лить спектрофотометрически, так как окисленная форма индикатора ярко окрашена, а его лейко - вал трубка с краям, форма обычно бесцветна или имеет слабую окраску. [23]
При измерениях окислительного потенциала колориметрическим методом для получения термодинамического значения потенциала необходимо, чтобы система приходила в равновесие с индикатором. Для этого при измерениях окислительного потенциала в системах, в которых процессы окисления - восстановления осуществляются с участием водорода и, в особенности, кислорода, так же как и при электрометрическом измерении, требуется введение катализаторов, ускоряющих окислительно-восстановительную реакцию. Кроме того, необходимо, чтобы при измерениях потенциала систем, в которых процесс восстановления осуществляется водородом, окисленная форма индикатора достаточно быстро восстанавливалась водородом. [24]
Необходимым условием определения окислительного потенциала колориметрическим методом является быстрое установление равновесия между индикатором и исследуемой системой. Поэтому в системах, в которых процессы окисления-восстановления осуществляются с участием водорода или кислорода, измерение окислительных потенциалов следует производить в присутствии катализаторов, ускоряющих окислительно-восстановительную реакцию. Кроме того, необходимо, чтобы при измерениях потенциала систем типа ( II), в которых процесс восстановления осуществляется водородом, окисленная форма индикатора достаточно быстро восстанавливалась. Аналогично для окислительно-восстановительных систем типа ( III) измерения потенциала в принципе возможны только в случае, если восстановленная форма индикатора быстро окисляется кислородом. Это требует, в свою очередь, тщательного удаления примесного кислорода, концентрация которого должна быть меньше, чем равновесная концентрация кислорода, выделяемого в течение окислительно-восстановительной реакции. [25]
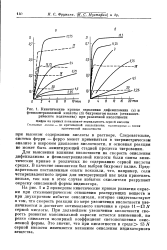 |
Кинетические кривые окисления дифениламина ( а и фенилантраниловой кислоты ( б бихроматом калия ( стехиомет. [26] |
Для выяснения влияния кислотности на скорость окисления дифениламина и фенилантраниловой кислоты были сняты кинетические кривые в различных по содержанию серной кислоты средах. В качестве окислителя был выбран бихромат калия. Предварительно поставленные опыты показали, что, например, соли четырехвалентного церия для интересующей нас цели применять нельзя, так как в этом случае избыток окислителя разрушает окраску окисленной формы индикатора. [27]
Титрование Hgn аскорбиновой кислотой ( восстановление до металлической ртути) проводят в слабоазотнокислой среде при 60 С в отсутствие С1 - - ионов. После того как добавляют половину титранта, раствор обесцвечивается ( вследствие окончания реакции 2Hga - Hg); это дает возможность вычислить ориентировочно количество титранта, необходимого для полного восстановления ртути до металла. Раствор остается бесцветным несколько секунд. При дальнейшем добавлении раствора аскорбиновой кислоты выделяется металлическая ртуть и возвращается первоначальная окраска окисленной формы индикатора. [28]
Титрование Hg11 аскорбиновой кислотой ( восстановление до металлической ртути) проводят в слабоазотнокислой среде при 60 С в отсутствие С1 - - ионов. После того как добавляют половину титранта, раствор обесцвечивается ( вследствие окончания реакции 2Hga - v Hg); это дает возможность вычислить ориентировочно количество титранта, необходимого для полного восстановления ртути до металла. Раствор остается бесцветным несколько секунд. При дальнейшем добавлении раствора аскорбиновой кислоты выделяется металлическая ртуть и возвращается первоначальная окраска окисленной формы индикатора. [29]
В качестве индикатора применяют бесцветный раствор дифениламина, котррый при окислении переходит в дифенилбензидин-виолет сине-фиолетового цвета. Бихромат калия окисляет дифениламин и смесь приобретает красно-бурую окраску. При титровании солью Мора шестивалентный хром восстанавливается в трехвалентный. В результате цвет раствора переходит в синий, а к концу титрования - в сине-фиолетовый. Когда же хром будет оттитрован, последующее добавление соли Мора вызывает переход окисленной формы индикатора в восстановленную ( бесцветную); появляется зеленая окраска, которую придают раствору ионы трехвалентного хрома. [30]
Страницы: 1 2