Другая кристаллическая форма
Cтраница 1
Другая кристаллическая форма принадлежит ромбоэдрической системе ( призмами), образуется также при возгонке, когда кристаллы осаждаются на нагретые поверхности, и при кристаллизации из щелочных растворов. [1]
Было сообщено о существовании двух других кристаллических форм поливинилиденфторида, обозначенных как формы I и II или ( 3 - и у формы соответственно. Осаки и Ишида [ 174], а также Преет и Луча [ 189, 190] переводили кристаллическую форму II в кристаллическую форму III путем твердофазного превращения при отжиге. Было показано, что обратное превращение в кристаллическую форму II, для которого, согласно Хасегава и др. [85], необходима термообработка, происходит после полного разрушения кристаллов форм I и III и последующей рекристаллизации. Оценка относительной устойчивости различных кристаллических форм осложнена вследствие распределения кристаллов по размерам и возможности необратимых переходов кристалл-кристалл, сопровождающихся изменением конформации макромолекул. [2]
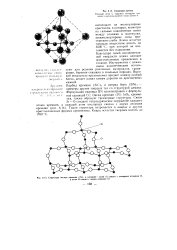
Большая стабильность икосаэдров по сравнению с другими кристаллическими формами ( рис. 1.6) сохраняется до кластеров из 2000 атомов. [3]
 |
Структура алмаза.| Структура оксида кремния ( IV, в которой - атом Si связан с четырьмя атомами О. [4] |
Такая структура встречается в кварце и других кристаллических формах кремнезема. Кварц остается твердым вплоть до 1700 С. [5]
При достижении предельных условий наступает переход в другую кристаллическую форму, причем границы этого перехода определяются, как и границы настоящего изменения агрегатного состояния, а сам переход сопрово-ждается тепловым эффектом. Кроме того, каждая из полиморфных кри-сталлических форм обладает отличной, свойственной только ей, упру-гостью паров и растворимостью. [6]
Гревер ( 1964) объясняют это различие присутствием другой кристаллической формы, выпадающей из раствора. Плавление и переход из одной кристаллографической модификации в другую наблюдаются в области температур от 370 до 410 К. [7]
Структура кварцевого стекла очень напоминает структуру кварца и других кристаллических форм двуокиси кремния. Почти каждый атом Si находится в центре тетраэдра из четырех атомов кислорода, и почти каждый атом кислорода является общим для двух таких тетраэдров. Однако строение пространственной решетки из таких тетраэдров в стекле не столь упорядочено, как в кристаллических формах двуокиси кремния, и лишь очень малые участки напоминают кварц или кристобалит и тридимит, точно так же как жидкая двуокись кремния при температуре, превышающей точку плавления кристаллических форм, несколько напоминает по своему строению соответствующие кристаллы. [8]
По-видимому, этот элемент необходим для образования гексамера и других кристаллических форм инсулина, в виде которых происходит депонирование инсулина р клетками поджелудочной железы [ Maske P. Изучение влияния цинка на активность инсуляриого аппарата показало связь между содержанием в нем цинка и его функциональным состоянием. Включение цинка в инсулин пролонгирует его физиологическое действие и гипогли-кемическое состояние. С учетом этого явления был приготовлен препарат протаминцинкинсулин, оказывающий пролонгированное гипогликемическое действие. Нарушение гомеостаза глюкозы в плазме крови при недостаточности цинка у крыс, описанное ранее, в более поздних опытах не подтвердилось [ Che-sters J. [9]
Здесь же в некоторых случаях приводятся температуры перехода вещества в другую кристаллическую форму. [10]
Здесь же в некоторых случаях приводятся температуры перехода вещества в другую кристаллическую форму. [11]
Из молекул тримера в основном состоит а-форма 8Оз - Структурной основой других кристаллических форм 5Оз являются зигзагообразные цепи, изолированные друг от друга у - SOj, соединенные в плоские сетки у у - 8Оз или в пространственные структуры у 5 - SOs. Окружение серы кислородом в полимерах SOs тетраэдрическое. Полимерные структуры SOs легко переходят друг в друга, и твердый 8Оз обычно состоит из смеси различных форм, относительное содержание которых зависит от условий получения образца. [12]
Применяемый в хроматографии оксид алюминия в основном содержит у-форму и небольшие количества других кристаллических форм, которые обладают близкими сорбционными свойствами. Если нагреть оксид алюминия до 1100 С и выше, то все модификации переходят в а-форму, которая хроматографически инертна. Это, по-видимому, объясняется изменением структуры кристаллической решетки оксида алюминия и уменьшением удельной поверхности. [13]
Структура кварцевого стекла по своему общему характеру очень напоминает структуру кварца и других кристаллических форм двуокиси кремния. Почти каждый атом Si находится в центре тетраэдра из четырех атомов кислорода, и почти каждый атом кислорода является общим для двух таких тетраэдров. Однако строение пространственной решетки из таких тетраэдров в стекле не столь упорядоченно, как в кристаллических формах двуокиси кремния, и лишь очень малые участки напоминают кварц, причем прилегающие к ним участки могут походить на кр истова л иг или тридимит, точно так же как жидкая двуокись кремния при температуре, превышающей температуру плавления кристаллических форм, несколько напоминает по своему строению соответствующие кристаллы. [14]
Из кристаллической полиморфной формы транс-коричной кислоты ( называемой а-формой) образуется одна из стереоизомерных труксиловых кислот ( а-трук-силовая кислота); из другой кристаллической формы ( 3) той же кислоты образуется стереоизомер труксиновой кислоты, называемый ( З - труксиновой кислотой. Существуют пять труксиловых и шесть груксиновых кислот ( геометрических изомеров, отличающихся положением групп СвН8 и СООН относительно циклобутанового кольца); все они известны. Некоторые из этих изомеров являются рацемическими смесями, которые можно расщепить на оптические антиподы. Труксиловая и ( 3-труксиновая кислоты были также выделены из листьев кока ( Erylhroxylon coca), в которых они связаны с алкалоидами, сопутствующими кокаину. [15]
Страницы: 1 2 3