Неионизированная форма
Cтраница 2
К этому можно добавить четвертое условие: если ионизированное вещество не имеет неионизированной формы, с. [16]
Зависимости здесь более сложные, так как речь идет об одновременном разделении ионизированных и неионизированных форм азуленов. [17]
Недостатком воды как ионизирующего растворителя для органических соединений является низкая растворимость в ней неионизированных форм этих соединений. За исключением этого ограничения, вода - уникальный эффективный ионизирующий растворитель, что связано прежде всего с ее высокой диэлектрической проницаемостью ( е 80), а также со способностью сольватировать ионы. Чем выше диэлектрическая проницаемость ( полярность) растворителя, тем ниже электростатическая энергия любой пары ионов, находящихся в нем, и, следовательно, тем легче возникают такие пары ионов, тем выше их стабильность в растворе и тем меньше склонность к взаимодействию друг с другом. [18]
Очевидно, что эти данные нельзя объяснить только исходя из реакции с участием неионизированной формы субстрата, катализируемой ионами гидроксония, и реакции дважды ионизированных молекул, катализируемой ионами гидроксила. [19]
Достигаемая таким путем значительная стабилизация аниона увеличивает его концентрацию в равновесной смеси с неионизированной формой. Аналогичное взаимодействие невозможно в / г-нитробензойной кислоте и ее анионе, а также в м-нитрофеноле и его анионе. Поэтому n - нитрофенол оказывается более сильной кислотой, чем можно было бы ожидать на основании свойств и-нитробен-зойной кислоты или л-нитрофенола. [20]
Таким образом, следует ожидать, что равновесие в этой системе будет более смещено в сторону неионизированной формы, чем в системе метановая кислота - метаноат-анион. Однако степень структурного изменения, проявляющегося в такой небольшой молекуле, как метановая кислота, при замене атома водорода на метильную группу настолько велика, что приведенное выше простое объяснение может и не отражать основные причины наблюдаемого различия. Вполне возможно, что различная способность к сольватации в случае этих двух кислот объясняется заметным различием форм их молекул, а также различным распределением заряда. [21]
Кислый характер активного метиленового соединения можно приписать резонансной стабилизации аниона енола, поскольку стабилизирующее взаимодействие с неионизированной формой невозможно. [22]
Жидкостная экстракция особенно удобна при извлечении из воды неполярных и малополярных веществ, присутствующих в водных растворах в неионизированной форме. В частности, она широко применяется для группового извлечения ПАУ. Одновременно достигается высокая степень их концентрирования и отделения от полярных ( водорастворимых) веществ. Видно, что для извлечения ПАУ применяют неполярные или малополярные растворители. [23]
Кислый характер активного метиленового соединения можно прииисат ], резонансной стабилизации аниона енола, поскольку стабилизирующее взаимодействие с неионизированной формой невозможно. [24]
В отличие от фенолфталеина, с которым он сходен по своему строению и реакции образования, флуоресцеин окрашен как в неионизированной форме, так и в виде двунатриевой соли. [25]
Константу равновесия меркурирования бензола в условиях окислительного нитрования определять трудно, поскольку азотная кислота при этом находится частично в ионизированной и частично в неионизированной форме. [26]
Однако в большинстве случаев при анализе лекарственных средств приходится jmeTb дело с такими слабыми осномниями у, которых в водном растворе равновесие сдвинуто в сторону неионизированной формы. Они образуют соли только с сильными кислотами. Поэтому после удаления соединений кислого и нейтрального характера к полученному раствору добавляют щелочь и создают в нем избыток гидроксильных ионов. При этом основания в виде неионизированной формы могут быть количественно извлечены из раствора. [27]
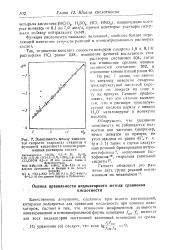 |
Зависимость между константой скорости гидролиза сахарозы и функцией кислотности концентрированных растворов кислот. [28] |
Единственное допущение, сделанное при выводе соотношений, которыми пользуются для сравнения кислотности при помощи индикаторов, состоит в том, что отношение коэфициентов активности ионизированной и неионизированной формы основания / шг / в является для всех индикаторов постоянной величиной независимо от среды. [29]
Однако хотя перечисленные альдегиды и кетоны и не могут ионизироваться с образованием енолят-ионов, они могут участвовать в перекрестных конденсациях, выступая в них в виде неионизированных форм. [30]
Страницы: 1 2 3 4