Диссоциация - ионит
Cтраница 2
Уменьшение сорбции К и Na в изученных растворителях, вероятно, обусловлено уменьшением поглотительной способности сорбентов. Последнее является следствием уменьшения диссоциации ионита и образования при низких ДП и высоких кислотностях раствора больших квазимолекул, более сложных чем ионные двойники. [16]
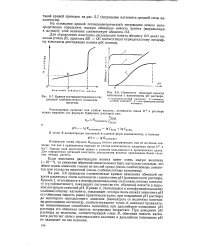 |
Кривая потенциометрического титрования слабокислотного катионита щелочью.| Изменение обменной емкости катионитов с изменениием рН раствора. [17] |
Для определения истинной константы диссоциации ионитов предложены более сложные методы расчета. [18]
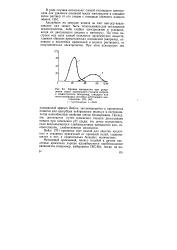 |
Кривые вымывания при разделении смеси электролита ( хлорид натрия и неэлектролита ( например, глицерин или полиглицериды способом отстающего электролита. [19] |
Вейсса, заключающийся в применении ионитов для адсорбции нейтральных молекул в состоянии, когда ионообменные свойства смолы блокированы. Последнее достигается путем изменения степени диссоциации ионита при изменении рН среды; это легко осуществить, если воспользоваться слабокислотным катионитом или, соответственно, слабоосновным анионитом. [20]
Стремление ионной атмосферы Н - катионита к рассеянию в растворителе и способность ее в процессе такого рассеяния совершать работу повышения концентрации водородных ионов в пограничном электронейтральном растворе кислоты может трактоваться как упругость ионной атмосферы Н - катионита. Величина этой упругости в момент возникновения ионной атмосферы ( или, что то же самое, в момент ее исчезновения, так как процесс диссоциации ионита является обратимым) можетбытьназвана упругостью диссоциации ионита. [21]
Стремление ионной атмосферы Н - катионита к рассеянию в растворителе и способность ее в процессе такого рассеяния совершать работу повышения концентрации водородных ионов в пограничном электронейтральном растворе кислоты может трактоваться как упругость ионной атмосферы Н - катионита. Величина этой упругости в момент возникновения ионной атмосферы ( или, что то же самое, в момент ее исчезновения, так как процесс диссоциации ионита является обратимым) можетбытьназвана упругостью диссоциации ионита. [22]
Различная степень диссоциации ионитов зависит в основном от характера функциональных групп, поэтому последние иногда делят на сильно - и слабокислотные и сильно - и слабоосновные. Такая классификация правомерна при условии, что у сравниваемых ионитов остальная часть молекулы ( скелет ионита) имеет сходное строение. Необходимо иметь в виду, что, помимо характера функциональной группы, на степень диссоциации ионита влияет ( иногда весьма резко) также и структура скелета, вызывая понижение или повышение кислотных и основных свойств функциональных групп. [23]
Как правило, набухание ионита протекает обратимо и характеризуется равенством между осмотическим давлением внутреннего раствора, с одной стороны, и натяжением эластичной сетки полимера, с другой. Осмотическое давление почти полностью обусловлено противоионами. Можно предположить поэтому, что обмен противо-ионов оказывает существенное влияние на процесс набухания. При этом решающее значение имеет число осмотически активных ионов на единицу веса ионита. Следовательно, однозарядные про-тивоионы должны вызывать более сильное набухание, чем многозарядные. Можно также утверждать, что добавление электролита к внешнему раствору должно приводить к уменьшению набухания, если степень диссоциации ионита считать постоянной. Проведенные Самуэльсоном [102, 104] эксперименты над сульфированными катионитами различных типов показали, что указанные закономерности, за редкими исключениями, хорошо выполняются. [24]
Страницы: 1 2