Диссоциация - молекула
Cтраница 1
Диссоциация молекул на атомы резко повышает их реакционную способность. Общее давление в системе равно 1 атм. [1]
Диссоциация молекул легче происходит в полярных жидкостях, чем в неполярных. Ввиду того что энергия диссоциации полярных жидкостей значительно меньше, чем неполярных, их удельная проводимость существенно выше. В неполярных жидкостях молекулы основного вещества практически не диссоциируют на ионы, и их электропроводность обусловлена примесями, особенно полярных веществ. [2]
Диссоциация молекул на ионы ( обычно называемая электролитической диссоциацией) приводит к увеличению числа частиц в растворе. Аво-гадро, то вследствие диссоциации число частиц ( молекул и ионов) станет больше. Следовательно, возрастет и концентрация раствора, измеряемая числом частиц в единице объема. [3]
Диссоциация молекул на ионы ( обычно называемая электролитической диссоциацией) приводит к увеличению числа частиц в растворе. Авогадро, то вследствие диссоциации число частиц ( молекул и ионов) станет больше. Следовательно, возрастет и концентрация раствора, измеряемая числом частиц в единице объема. [4]
Диссоциация молекул в результате теплового воздействия может происходить или за счет поглощения молекулами энергии иди же за счет столкновений молекул. [5]
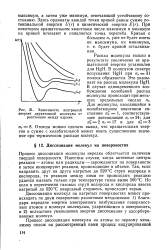 |
Зависимость внутренней. [6] |
Диссоциация молекул на нагретых поверхностях может происходить по двум совершенно различным механизмам: 1) благодаря передаче энергии электронного возбуждения поверхностных атомов и молекул молекулам, ударяющимся о поверхность, и 2) вследствие уменьшения энергии диссоциации у адсорбированных молекул. [7]
Диссоциация молекул в результате теплового воздействия может происходить или за счет поглощения молекулами энергии или за счет столкновений молекул. Диссоциация молекул в результате поглощения энергии принципиально ничем не отличается от процесса фотохимической диссоциации. [8]
Диссоциация молекул на нагретых поверхностях может происходить по двум совершенно различным механизмам: 1) вследствие передачи энергии электронного возбуждения поверхностных атомов и молекул молекулам, ударяющимся о поверхность, и 2) вследствие уменьшения энергии диссоциации у адсорбированных молекул. [9]
Диссоциации молекул соответствует возникновение сплошного спектра. На рис. 119 показан спектр поглощения паров иода, при 4995 А наблюдается переход полосатого спектра в сплошной, что как раз и соответствует процессу диссоциации молекул иода. [10]
Диссоциация молекул О2 на атомы становится заметной лишь при 2000 С. [11]
 |
Величина искрового промежутка в комнатном воздухе. [12] |
Диссоциация молекулы на электрополярные части, вызванная ударом v она, состоит в том, что один из заключенных в недрах молекулы электронов выбрасывается наружу, и сама молекула приобретает эквивалентный электрону положительный заряд. Процесс этот сопровождается электромагнитным возмущением эфирной среды. Таким образом, слой газа, прилегающий к катоду, - первый катодный слой ( рис. 398, стр. Новообразованные положительные ионы будут немедленно привлечены к поверхности катода, где и отдадут свой заряд; электроны под действием сил отталкивания, исходящих от катода, направятся в противоположную сторону вакуумтрубки; наряду с этими электронами в том же направлении будут двигаться и те электроны, которые благодаря ударам положительных ионов о поверхность катода окажутся вырванными из вещества катода. [13]
Диссоциация молекулы под действием удара электрона обычно следует непосредственно за возбуждением и похожа на рассмотренный уже процесс фотодиссоциации. В обоих случаях происходит переход молекулы или на кривую отталкивания, или в такую область кривой устойчивого возбуждения, в которой энергия молекулы оказывается больше энергии диссоциации на соответствующие продукты. [14]
Диссоциация молекул на нагретых поверхностях может происходить по двум совершенно различным причинам: 1) в результате передачи энергии электронного возбуждения поверхностных атомов и молекул молекулам, ударяющимся о поверхность, и 2) вследствие уменьшения энергии диссоциации адсорбированных молекул на атомы. [15]
Страницы: 1 2 3 4