Диссоциация - последнее
Cтраница 3
Особенности кинетики химических реакций, происходящих под действием излучений, в основном обусловлены тем, что наиболее трудная стадия химического процесса, представляющая собой взаимодействие между молекулами ли диссоциацию последних, заменяется взаимодействием молекул с валентно-ненасыщенными частицами ( атомами, радикалами, ионами), а также взаимодействием этих частиц между собой. [31]
При взаимодействии расплава припоя с окисной пленкой на основном металле образование химической связи между атомами металлов и окислами становится возможным, когда атомы металла передают свои электроны ионам кислорода окисла в процессе диссоциации последнего. Процесс диссоциации окислов сопровождается разрывом связей кислород - металл. Кислород, забирая электроны, образует в жидком металле комплексы О - - - Ме, локализуя на себе валентные электроны разорванных химических связей. [33]
Ясно, что в конце концов установится равновесие, при котором сколько ионов № в единицу времени будет связываться в молекулы HCN, столько же их будет появляться в растворе в результате диссоциации последних. При этом равновесии концентрация ионов ОН будет, очевидно, значительно превышать концентрацию ионов Н и потому раствор KCN должен иметь щелочную реакцию. [34]
Однако трудно допустить независимость скорости движения ионов от концентрации раствора сильного электролита. При диссоциации последнего образуется весьма много ионов, которые в силу этого ( особенно в более концентрированных растворах) находятся настолько близко друг к другу, что между ними должны действовать силы электростатического притяжения и отталкивания. [35]
В согласии с этим механизмом обмен идет между S - S36O3 и SO3, но не между S35 - SO3 и SO3 Эмис и Уилард [724] изучили кинетику этого обмена и нашли, что скорость его пропорциональна произведению концентраций сульфита и тиосульфата. Это исключает диссоциацию последнего на S SO3 -, как путь обмена. Обмен тиосульфата с HS35 - сульфидов идет медленнее, чем с сульфитом, однако оба имеют одинаковую энергию активации [718], что можно объяснить общей медленной ступенью разрыва связи S - SB комплексе. [36]
Поскольку данная теория предполагает, что между реагирующими веществами и переходным комплексом существует равновесие, задача по существу ставится так же, как и при расчете констант равновесия для реакций изотопно замещенных молекул. Колебания переходного комплекса приводят к диссоциации последнего на продукты реакции, поэтому соответствующая частота оказывается мнимой и - отношение констант скорости, а также отношение констант равновесия для молекул, содержащих различные изотопы определенного элемента, зависят от отношения этих частот. Отсутствие информации о квантовых состояниях переходного комплекса создает определенные трудности, которых часто можно избежать используя некоторые приближения, так как для переходных комплексов, содержащих различные изотопы какого-либо элемента, необходимо знать только отношение функций распределения. В худшем случае максимальное значение можно оценить, предполагая, что изотопный атом не входит в состав переходного комплекса. При замещении атома Н1 на Н3 изотопный эффект такой реакции равен 60; для атомов С12 и С14, а также I127 и I131 эта величина равна 1 5 и 1 02 соответственно. [37]
Следует учесть еще, что, применяя в качестве осадителей слабые электролиты, можно регулировать концентрацию осаждающего иона, повышая концентрацию одного из ионов, участвующих в равновесии. Так, при осаждении А13 - иона аммиаком можно регулировать диссоциацию последнего с помощью добавок аммоний-яых солей. [38]
Буферность твердой фазы почвы обусловливается в основном двумя факторами: количеством почвенных коллоидов и составом поглощенных катионов. Большое значение имеет также энергия поглощения водородных ионов почвенными коллоидами и степень диссоциации последних. Опыт показывает: чем больше данная почва содержит органического вещества, тем выше ее буферное действие. [39]
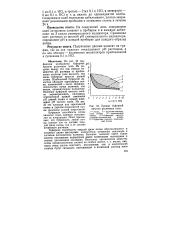 |
Кривые буферной емкости различных почв. [40] |
Буферная способность твердой фазы почвы обусловливается в основном двумя факторами: количеством почвенных коллоидов и составом поглощенных катионов. Большое значение имеет также энергия поглощения водородных ионов почвенными коллоидами и степень диссоциации последних. [41]
 |
Кривые титрования. [42] |
Буферность твердой фазы почвы обусловливается в основном двумя факторами: количеством почвенных коллоидов и составом поглощенных катионов. Большое значение имеют также энергия поглощения водородных ионов почвенными коллоидами и степень диссоциации последних. Опыт показывает: чем больше данная почва содержит органического вещества, тем выше ее буферное действие. [43]
Один из них, например, связан с применением двойных и тройных смесей слабых кислот с сильной кислотой. Сильная кислота ( например, НС1) в растворе со слабыми кислотами подавляет диссоциацию последних, на чем и основано замедленное вступление в реакцию молекул слабой кислоты, так как молекулы таких кислот, не подвергшиеся диссоциации, не реагируют с породой практически вплоть до полной нейтрализации сильной кислоты. В качестве слабых кислот используют органические кислоты - уксусную и муравьиную. Добавление в 15 % - ную НС1 только 8 % ( по объему) 90 % - ной муравьиной кислоты увеличивает время нейтрализации в 3 5 раза, а добавка в 15 % - ную НС1 10 % 100 % - ной уксусной кислоты может увеличить время нейтрализации до 8 5 раза. [44]
Дезактивация возбужденных молекул Б конденсированных системах, как было указано выше, происходит значительно быстрее благодаря большей частоте столкновений. Энергия возбуждения может передаваться от сравнительно стабильных молекул к менее стабильным, вызывая диссоциацию последних. [45]
Страницы: 1 2 3 4