Функция - кислотность - среда
Cтраница 1
Функция кислотности среды является эквивалентом величины pll для достаточно концентрированных растворов кислот, в которых концентрация ионов водорода перестает характеризовать кислые свойства среды. [1]
Следовательно, Igk3 линейно зависит от функции кислотности среды, причем угловой коэффициент наклона прямой линии, изображающей эту зависимость, равен минус единице. [2]
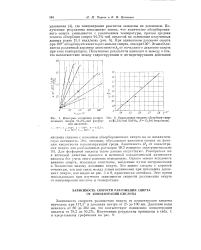 |
Изотермы абсорбции изопро - [ IMAGE ] Определение теплоты абсорбции спир-пилового спирта 94 3 % - ной фосфор - та 94 3 % - ной НзРОц. /. 15 500 ккал / моль. ной кислотой. [3] |
Это, очевидно, обусловлено влиянием спирта на функцию кислотности катализирующей среды. Для фосфорной кислоты такие данные отсутствуют. Разобраться же в истинной кинетике процесса и истинной каталитической активности кислоты без учета этого влияния невозможно. Однако можно исключить влияние спирта, используя константы, найденные путем экстраполяции к бесконечно малому давлению спирта. Это можно сделать с хорошей точностью, так как связь между этими величинами при небольших давлениях спирта, как видно из рис. 5 и 9, практически линейная. [4]
Побочный процесс - образование алкилкислоты - приводит к изменению функции кислотности среды. [5]
Другими словами, концентрация иона карбония пропорциональна упругости паров олефина и функции кислотности среды. Обратим внимание на то, что здесь ион карбония рассматривается не как продукт переходного состояния ( переходный комплекс), которому обычно приписывается то свойство, что его концентрация не зависит от температуры, а как устойчивое соединение с определенной теплотой образования. [6]
Зависимость К от концентрации кислоты, а следовательно, и от функции кислотности среды легко может быть определена экспериментально. [7]
Таким образом, показано, что скорость разложения спирта изменяется пропорционально первой степени функции кислотности катализирующей среды. [8]
Низкая основность 1 4 - ДГП требует применения для гидролиза сильно кислой среды ( функция кислотности среды Б 0 62 для N-замещенных ДГП; HO - 0 94 для NH-ДГП), что в некоторых случаях вызывает деструкцию CQQR-rpyrm циююгексено-на, При рециклизации N-замещенных эфиров Ганча наряду с циклогексеноном обнаружено незначительное количество продукта N-деалкжлирования ( деаршшрования), что свидетельствует об образовании также и N-протонированной формы ДГП в условиях реакции. Следует отметить что те же самые производные циклогексенона образуются и при гидролизе алкиламино-циклогексадиенов, полученных нами в условиях реакции Ганча. [9]
Колориметрический метод определения рН растворов основан на использовании кислотно-основных индикаторов, окраска растворов которых является функцией кислотности среды. Окраска изменяется в результате изменения относительной доли ионизированной ( Ind) и неионизированной ( Hind) форм, Ямакс поглощения которых различно. [10]
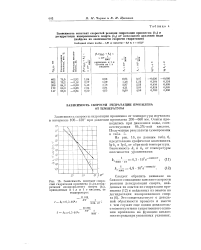 |
Зависимость констант скоростей гидратации пропилена ( / С [ идегид-ратации изопропилового спирта ( &2, приведенных к 1 л и 1 г кислоты, от температуры. [11] |
Это свидетельствует о детальной обратимости процесса и вместе с тем служит еще одним доказательством отсутствия существенного влияния пропилена на функцию кислотности среды при указанных условиях. [12]
На примере изучения реакций гидролиза сахарозы в концентрированных растворах сильных кислот было показано [16], что каталитическая константа скорости однозначно определяется функцией кислотности среды вне зависимости от других специфических свойств кислот. [13]
Во многих случаях это явление может быть объяснено с количественной точностью, если принять, согласно Гаммету, за меру каталитической активности кислот так называемую функцию кислотности среды. [14]
Исследование реакции поликонденсации аценафтена с формальдегидом27 в гомогенной среде вода - уксусная кислота в присутствии катализатора ( серная кислота) показало, что скорость реакции зависит от функции кислотности среды, хотя и не прямо пропорциональна ей. [15]
Страницы: 1 2