Функция - гаммет
Cтраница 1
Функция Гаммета Я0 близка к рН в разбавленных растворах, когда можно пренебречь разницей между концентрацией и активностью растворенных веществ. Однако в концентрированных растворах разница между Яо и рН будет весьма существенна, поскольку второй член правой части уравнения (3.74) в этом случае нулю не равен. [1]
Функция Гаммета Яо близка к рН в разбавленных растворах, когда можно пренебречь разницей между концентрацией и активностью растворенных веществ. Однако в концентрированных растворах разница между На и рН будет весьма существенна, поскольку второй член правой части уравнения (3.74) в этом случае нулю не равен. [2]
Очевидно, что для определения функции Гаммета необходимо располагать серией индикаторов, которая охватывала бы широкую область кислотности. Функции Гаммета полезны для оценки относительной кислотности сред различного состава и природы и корреляции скоростей реакций в различных растворителях. [3]
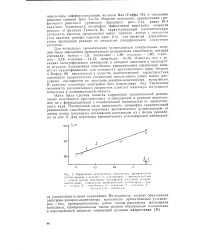
Этот результат заставляет сомневаться в пригодности функции Гаммета как функции кислотности, поскольку, вероятно, в этих растворах скорость жзмшения Ъ по абсолютной величине, сравнима или даже меньше скорости изменения г / в / г / вн при изменении состава среды. Косвенным подтверждением этому могут служить результаты работы [59], в которой показано, что в уксусноводных растворах редокс-функция R0 ( H) - lg ( й-г / рег / г / гес), так же как и функция кислотности Гаммета, в области средних составов возрастает по мере увеличения концентрации уксусной кислоты. Растворимость ферроцена и, следовательно, г / рес в бинарной системе Н20 - СН3СООН меняется на четыре порядка, причем очень сильно именно в области средних составов. [4]
 |
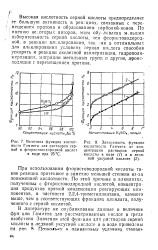
Функция Гаммета водных растворов хлорной кислоты при 25 С. [5] |
Сравнение относительной силы кислот на основании функций Гаммета также приводит к ряду, в котором хлорная кислота занимает первое место. [6]
В литературе не опубликованы данные о величине функции Гаммета для рассматриваемых кислот в среде изобутана. [8]
Реакция подвержена специфическому катализу водородными ионами; в области средней кислотности она пропорциональна функции Гаммета Н0 ( см. разд. [9]
Так как для многих физико-химических исследований, проводимых в сильно кислых растворах с большим содержанием серной кислоты, необходимо точно знать функцию Гаммета, то в табл. 3 - 6 мы приводим ее значение для некоторых молярных ( или процентных) концентраций серной кислоты в воде. [10]
Рассмотрены факторы, влияющие на ионные равновесия в неводных растворителях, образование ионных пар в растворителях с малым значением диэлектри ческой проницаемости, ход кривых титрования, а также вкратце функции Гаммета. [11]
Тем не менее совсем недавно Анбаром и Хартом [30] была предпринята первая попытка получить такие корреляции, которые показали, что реакционная способность ароматических соединений по отношению к гидратирован-ным электронам находится в прямой связи с их реакционной способностью по отношению к нуклеофильным частицам, согласно функции Гаммета, о. Анбар и Харт считают гидратированный электрон самым простым и наиболее ре-акционноспособным нуклеофилом. [12]
Согласно Гаммету, Н0 характеризует потенциал раствора для переноса протона к такому основанию В, для которого под влиянием среды / вн / / в изменяется так же, как аналогичное отношение для индикаторов [ 17, с. Функция Гаммета обозначается через Н0, так как индикаторы основания не имеют заряда. Известны функции Н, для определения которых используется в качестве индикатора незаряженная кислота, а соответствующее ей основание имеет отрицательный заряд. Выбор концентрационной шкалы в уравнении (1.9) является очень важным. Обычно / 10 выражается в шкале молярных концентраций. [13]
Очевидно, что для определения функции Гаммета необходимо располагать серией индикаторов, которая охватывала бы широкую область кислотности. Функции Гаммета полезны для оценки относительной кислотности сред различного состава и природы и корреляции скоростей реакций в различных растворителях. [14]
Страницы: 1 2