Мольная функция
Cтраница 1
Мольная функция Гиббса ц обычно называется химическим потенциалом. Причина появления такого названия состоит п следующем. В механических системах направление спонтанного изменения может быть предсказало просто определением потенциала вблизи данной частицы. Частицы, первоначально находящиеся в стационарном состоянии, имеют естественную тенденцию плавно уменьшать свой потенциал, если над ними не производится работа. Когда рассматривается ансамбль молекул и когта энергия может рассеиваться в виде теплоты, ситуация не так проста. Тем не менее известно, что спонтанное изменение при постоянных Тир направлено в сторону минимума функции Гиббса для данной системы. Таким образом, функция Гиббса играет роль, аналогичную потенциалу, и по этой причине мольная функция Гиббса ( функция Гиббса для определенного числа молекул в ансамбле) названа химическим потенциалом. [1]
Любая парциальная мольная функция представляет собой, как известно, частную производную от интегральной функции ( Ф) по числу молей какого-либо ( - того компонента Hi при постоянном давлении, температуре и числах молей других компонентов раствора. [2]
Применяемые на практике мольные или парциальные мольные функции состояния Z, характеризующие термодинамическую систему, как правило, зависят от температуры, давления, а при реакциях в растворах также и от концентрации. В связи с этим, для того чтобы можно было табулировать данные о функциях состояния ( что удобно для сравнения), оказалось целесообразным выбрать некоторое стандартное состояние, исходя из которого можно расчетным путем перейти к функции состояния для любого конкретного состояния системы. [3]
То же применимо и к парциальной мольной функции Гиббса. [4]
В табл. III.3 приведена сводка наиболее важных аддитивных мольных функций и их обозначений. [5]
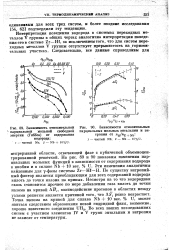 |
Зависимость относительной [ IMAGE ] Зависимости относительных парциальной мольной свободной парциальных мольных энтальпии и эн-энергии ( Гиббса от содержания тропии от ин / и мь. [6] |
На рис. 89 и 90 показаны изменения парциальных мольных функций в зависимости от содержания водорода в ниобии и в сплаве Nb 10 вес. По существу энтропийный фактор является преобладающим для всех содержаний водорода вплоть до точки излома на кривых. Несмотря на то что водородная связь становится прочнее по мере добавления газа вплоть до точки излома на кривой & Hi: взаимодействие протонов в областях между узлами решетки является причиной того, что & St резко возрастает. Точка излома на кривой для сплава Nb 10 вес. [7]
Такая аддитивная величина носит название функции Рао или мольной функции скорости звука. [8]
Согласно уравнениям (28.31) - (2.8.37) и определению (2.17.14) каждая парциальная мольная функция смешения Де. [9]
Согласно уравнениям (2.8.31) - (2.8.37) и определению (2.17.14) каждая парциальная мольная функция смешения Ае, относящаяся к одному и тому же компоненту к, выражается через химический потенциал смешения Дц. Поэтому задача сводится к отысканию функций типа Af. [10]
Химический потенциал компонента является также парциальной мольной величиной - парциальной мольной функцией Гиббса. [11]
Уже указывалось, что химический потенциал компонента является также парциальной мольной величиной-парциальной мольной функцией Гиббса. [12]
Другая удобная и часто применяемая форма представления фундаментальных уравнений для фазы связана с мольными функциями. [13]
В предлагаемой работе обосновывается несколько иной путь: вводится новый класс термодинамических функций ( парциальные мольные функции гетерогенных смесей), дополняющий аналогичное семейство функций гомогенных растворов. Это дополнение делает, по нашему мнению, метод термодинамики растворов более приспособленным для анализа сложных систем с чередующимися гомогенными и гетерогенными областями составов. Конкретные выводы и примеры ограничиваются двухкомпонент-ными двухфазными системами. [14]
Как видно, любая интегральная функция смешения и ее мольное значение могут быть вычислены через соответствующие парциальные мольные функции смешения компонентов. [15]
Страницы: 1 2