Молекулярная функция
Cтраница 3
Теории, называемые строгими, ставят своей задачей вывести все структурные характеристики, опираясь исключительно на сведения о молекулярных свойствах, потенциале межмолекулярного взаимодействия. Эти теории оперируют молекулярными функциями распределения, определяющими вероятность заданной конфигурации группы из двух или более частиц и позволяющими учесть корреляции в положениях частиц. Введенная ранее радиальная функция распределения может быть названа двухчастичной корреляционной функцией. [31]
Первый член в квадратных скобках соответствует ad, два последних - вр. Если мы вычисляем экранирование протона, то приближенные молекулярные функции обычно содержат только s - функцию атома водорода. [32]
Предположим, что в каждой из молекул, указанных в задаче 13.1, на каждом атоме имеется набор базисных функций, которые при операциях симметрии преобразуются подобно локальным декартовым координатам данного атома. К каким неприводимым представлениям группы симметрии каждой молекулы будут относиться молекулярные функции, которые могут быть построены нз таких базисных функций. [33]
При теоретическом исследовании структуры используются два подхода - формально строгий и модельный. Первый базируется на принципах статистической механики и приводит к строгим выражениям для молекулярных функций распределения, а через них - к уравнениям для расчета термодинамических свойств. В выражение для молекулярных функций распределения входит потенциал взаимодействия частиц, о котором мало что известно, даже в случае парных взаимодействий в простых системах. [34]
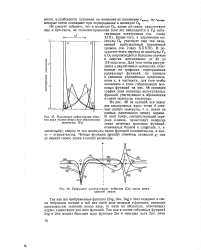 |
Наложение орбитальных облаков двух атомов фтора при образовании молекулы ( F2.| Гибридные молекулярные орбитали ( Ог вдоль межъядерной линии. [35] |
В результате этого переход от молекулы F2 к О2 сопровождается большим скачком в энергии диссоциации: от 40 до 118 ккал / моль. Для того чтобы рассуждения о двухатомных молекулах основанные на графиках перекрывания радиальных функций, не привели к слишком упрощенным представлениям и, в частности, для того чтобы напомнить о роли гибридизации волновых функций на рис. 48 приведен график хода волновых молекулярных функций, участвующих в образовании ст-связи молекулы кислорода. [36]
 |
Схема электронно-валентных состояний атомов в моносилицидах типа FeSi. [37] |
Координация такого ближайшего окружения соответствует симметрии Cu3 и очень хорошо описывается гибридными молекулярными орбитами spzdxzdyz [23]: расчетные углы между связями равны в этом случае 136 и 73, а реально наблюдаемые в кристаллах моносилицидов - 129 и 72 соответственно. Небольшое различие рассчитанных и наблюдаемых углов может быть качественно объяснено следующими соображениями. Поскольку в гибридных молекулярных функциях участвуют d - состояния, то для соответствующих атомов переходных элементов они могут легко реализоваться ( 4s4pz3dxz3dyz); в то же время для атомов кремния Sd-уровни нестабильны. Поэтому правильнее будет предположить, что атомы Si взаимодействуют с гибридными функциями металла путем перекрытия одной s и трех р атомных орбиталей. Это предположение, с одной стороны, объясняет указанное выше отличие углов между связями, а с другой - уменьшение длины одной из связей Me - Si по сравнению с тремя другими. [38]
Каждый из наборов, Л2 либо В2, может приводить к молекулярным функциям симметрии Eg. Эти два разных набора порождают ортогональные компоненты функций Ее. Для выбранного набора молекулярных функций построение полного набора требует использования одного и того же представления группы локальной симметрии. Выбор используемого представления может основываться на поведении базисной функции азота. [39]
Клетки и их органоиды - гетерогенные системы, существование и функционирование которых определяются межмолекулярными взаимодействиями невалентного характера. Исполнители почти всех молекулярных функций в клетках - белки - взаимодействуют с липидами и углеводами, с нуклеиновыми кислотами и с малыми молекулами. Взаимодействия эти преимущественно слабые, так как сильные взаимодействия создавали бы слишком жесткие и устойчивые структуры, лишенные молекулярной подвижности, необходимой для выполнения биологическими молекулами их разнообразных задач, включающих тонкую регуляцию химических реакций, компартментацию, установление градиентов концентрации. Перечислим виды слабых взаимодействий в биологических системах и охарактеризуем их. [40]
Каждый из наборов, Л2 либо В2, может приводить к молекулярным функциям симметрии Eg. Эти два разных набора порождают ортогональные компоненты функций Ее. Для выбранного набора молекулярных функций построение полного набора требует использования одного и того же представления группы локальной симметрии. Выбор используемого представления может основываться на поведении базисной функции азота. [41]
При теоретическом исследовании структуры используются два подхода - формально строгий и модельный. Первый базируется на принципах статистической механики и приводит к строгим выражениям для молекулярных функций распределения, а через них - к уравнениям для расчета термодинамических свойств. В выражение для молекулярных функций распределения входит потенциал взаимодействия частиц, о котором мало что известно, даже в случае парных взаимодействий в простых системах. [42]
Теперь на примере молекулы Н2 рассмотрим поведение электронных термов, в том числе и возбужденных. С этой целью молекулярную функцию строят в виде-линейной комбинации атомных функций. [43]
Для этого необходимо найти приближенную молекулярную функцию грмол, которая достаточно близка к истинной волновой функции системы. Выбор такой функции осуществляется чаще всего при помощи вариационного метода. [44]
Электронная пара, образующая химическую связь, как уже отмечалось, находится в общем пользовании двух ядер. В этом случае движение каждого электрона будет описываться новой волновой функцией, являющейся решением уравнения Шредингера для этой системы. Эта волновая функция отличается от атомных функций и называется молекулярной функцией, соответствующей определенной молекулярной орбитали. Молекулярные орбитали характеризуются определенными значениями полной энергии системы. В молекуле, как и в атоме, существует последовательность энергетических уровней. Однако строгое решение уравнения Шредингера для них получить не представляется возможным и поэтому прибегают к приближенным методам расчета, отличающимся друг от друга способом задания молекулярной волновой функции. [45]
Страницы: 1 2 3 4